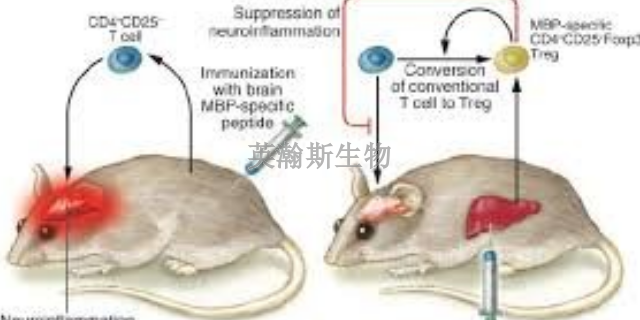
EAE模型的被动转移实验是研究其发病机制的**直接证据,也是研究EAE的***及预防措施的良好模型。将抗原***的PLP特异性T细胞转输给同一品系的正常大鼠或小鼠,也可引起EAE。MBP特异性自身反应性T细胞在MS的发病机制中也起着关键作用,T细胞必须先在外周活化,通过血管内皮细胞进入CNS才能致病。EAE的神经症状通常根据Kono等提出的标准分为5级。0级:无任何临床症状;1级:动物尾巴无力,2级:尾部无力+肢体无力,3级:肢体轻度麻痹,4级:肢体严重麻痹,被动翻身后不能复原;5级:濒死状态或死亡。eae模型是实验性自身免疫性脑脊髓炎模型的缩写。四川小鼠eae模型有哪些
随着多组学技术和成像手段的发展,EAE动物模型正在与转录组学、蛋白质组学、代谢组学以及体内***成像技术相结合,为系统性研究***免疫疾病提供新的可能。例如,通过单细胞RNA测序可以精细解析EAE过程中不同免疫细胞和神经胶质细胞的功能状态变化;而磁共振成像(MRI)和双光子显微镜技术则可实现疾病进程的动态、无创监测。这些新技术的引入,极大地提升了EAE模型在机制研究和药物评价中的信息量和精确度。EAE动物模型的构建需要专业动物模型构建平台。重庆大鼠eae模型有哪家eae模型的构建方法是什么?
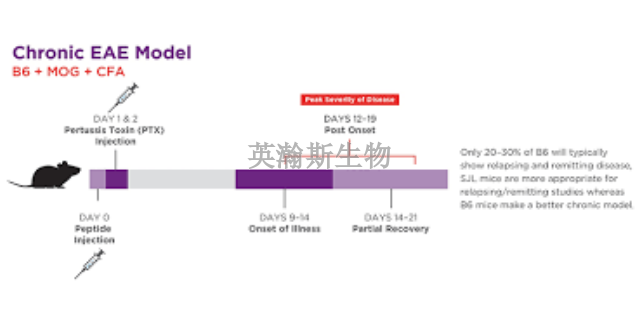
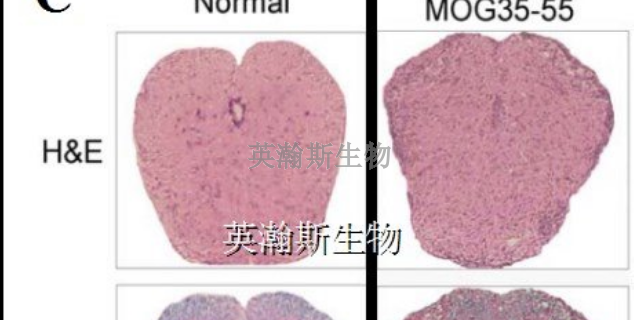
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突胶质细胞糖蛋白,髓鞘的一种微量成分,属于免疫球蛋白超家族成员之一。t也是特定表达于***系统(CNS)的自身抗原,诱导多发性硬化症的原发性脱鞘特征。MOG(35-55)是髓鞘少突胶质细胞糖蛋白的免疫优势表位,能够诱导强烈的T细胞和B细胞应激反应,具高度致脑炎性,能够诱导啮齿类动物的实验性白身免疫性脑脊髓炎(EAE)模型。EAE是**普遍的MS动物模型,具有MS许多的临床和病理生理学特征。单次注射MOG(35-55)能够产生一种复发-缓解型神经性疾病,表现出大量斑块状脱髓鞘病症。1-甲基-4-苯基-1,.2,3,6-四氢吡啶(MPTP)诱导的多巴胺神经元损伤模型,免疫接种MOG(35-55)能抑制该神经元的白发再生功能。
在EAE动物模型中,科学家们得以观察到神经系统受损后的再生和修复过程,这为神经修复研究提供了极为宝贵的重要线索。这一模型不仅模拟了多发性硬化症(MS)等神经系统疾病的病理过程,还使得我们能够直观地观察到受损神经系统的自我修复能力。通过观察EAE动物模型中神经元的再生、轴突的重新生长以及突触连接的重塑等现象,科学家们可以深入了解神经修复的内在机制。同时,这一模型也为研究神经修复提供了新的思路和方法,例如通过调控特定的信号通路或利用外源性因子来促进神经再生和修复。因此,EAE动物模型在神经修复研究领域中发挥着不可或缺的作用,有望为神经系统疾病的治疗带来**性的突破。EAE模型的发生也存在动物性别差异。
EAE动物模型(Experimental Autoimmune Encephalomyelitis,实验性自身免疫性脑脊髓炎)是研究***系统自身免疫性疾病,尤其是多发性硬化(Multiple Sclerosis,MS)**经典、应用*****的动物模型之一。该模型通过人为诱导机体对***系统髓鞘成分产生自身免疫反应,从而在实验动物中重现炎症细胞浸润、髓鞘脱失、轴突损伤以及神经功能障碍等关键病理特征。自20世纪中期建立以来,EAE模型在阐明MS的免疫发病机制、筛选潜在***靶点以及评估免疫调节药物疗效方面发挥了不可替代的作用。由于其可控性强、重复性相对较好,EAE已成为神经免疫学领域的“标准模型”,也是许多基础研究和转化医学研究的重要起点。小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功诱发EAE,在选择动物时需要寻找EAE模型的敏感动物。江苏真实的eae模型如何构建
EAE动物模型是研究MS病理过程、发病机制的重要途经,在临床神经免疫学的研究中具有重要意义。四川小鼠eae模型有哪些
近年来,随着研究重点从单纯免疫抑制转向神经保护和神经修复,EAE动物模型的应用范围进一步拓展。例如,研究者开始关注轴突损伤的早期发生机制、线粒体功能障碍、氧化应激以及少突胶质细胞前体细胞(OPCs)的分化与再髓鞘化过程。EAE模型为探索这些问题提供了动态观察的平台,使得研究者能够在疾病不同阶段采集样本,系统分析免疫炎症与神经退行性改变之间的因果关系,从而推动多发性硬化研究从“免疫疾病”向“免疫-神经综合疾病”的认知转变。四川小鼠eae模型有哪些