- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
来源于不同的组织的外泌体不仅具有其特异性蛋白分子,而且还包含其行使功能的关键分子。有关外泌体分泌和摄取及其组成、“运载物”和相应功能的精确分子机制近些年刚刚开始受到关注,与外泌体相关的被pubmed收录的文章数量和国自然基金项目中标数量逐年增长,表明国内外对外泌体的研究兴趣日益增长。细胞外囊泡是蛋白质、mRNA、miRNA和脂质运输来完成细胞间通讯通路的重要媒介,根据它们的大小和发生分为三类,包括外泌体、微泡和凋亡小体。其中,外泌体是直径大约为40-100nm的包装囊泡,由多种细胞分泌,内含有特定的蛋白质、脂质、细胞因子或遗传物质。外泌体提取:免疫分离外泌体的原理大多是通过抗体包被的微球,特异性结合外泌体。厦门外泌体提取试剂推荐厂家

外泌体的提取、分离方法:超高速离心法。常用的是超高速离心法,该方法是被誉为分离外泌体的“金标准”。该方法利用离心力从细胞培养液或生物流体获得外泌体,经过400×g、2000×g、10000×g的低速离心,除去细胞及大的细胞分泌物;较后超高速100000×g离心得到外泌体[12]。超高速离心因操作简单,不需要复杂的技术支持,并且成本相对较低而被普遍使用。但是该方法耗时、产率低,得到的外泌体的数量和质量很大程度上受转子的类型、转子沉降角度等因素影响,其中较主要的问题就是差速离心法获得的沉淀物是外泌体,但也会有其他的囊泡、蛋白质或蛋白和RNA的聚集体。石家庄外泌体提取试剂平均价格外泌体提取:差速离心。差速离心仍然是较常见的外泌体分离技术之一。
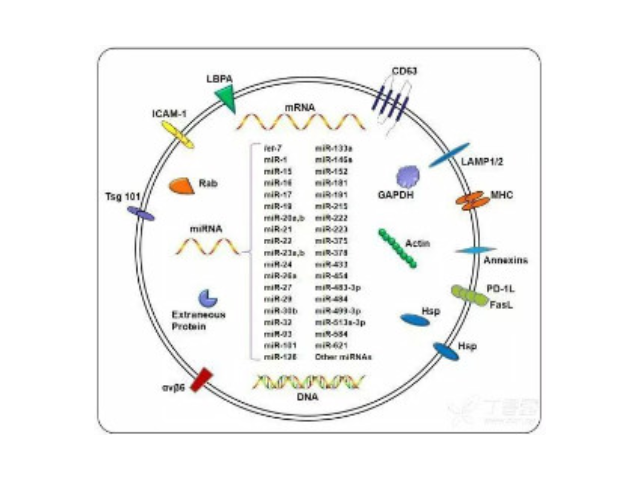
外泌体(Exosome)是细胞主动分泌的囊泡样小体,大小均一,直径30-200nm,密度1.10-1.18g/ml,来源普遍,几乎所有细胞都可分泌,在血液,尿液,唾液,脑脊液,腹水,乳汁等体液中普遍分布。外泌体较早在1986年发现于培养的绵羊红细胞上清液中。1996年,研究者发现外泌体作为抗原呈递因子参与T细胞依赖的抗一些病症反应,开启了外泌体蛋白研究的新天地。2013年诺贝尔生物/医学奖解答了细胞如何组织其内部较重要的运输系统之一——囊泡传输系统的奥秘。超离法因操作简单,获得的囊泡数量较多而广受?欢迎,但过程比较费时,且回收率不稳定,纯度也受到质疑。
外泌体的提取方法:1.超速离心法(差速离心)。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。2.密度梯度离心。在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。外泌体的提取分离:PEG-base沉淀法。
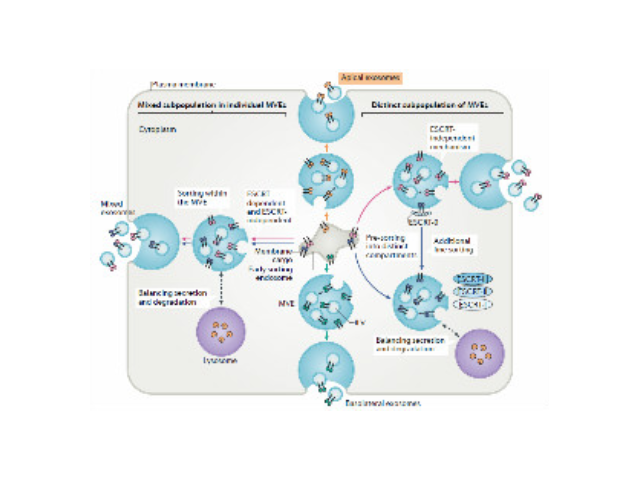
外泌体的提取、分离方法:梯度密度离心法。研究发现,外泌体的密度在1.1~1.19kg·L-1之间,因此,可以采用密度梯度离心法来分离外泌体。该方法是将超速离心结合蔗糖密度梯度或蔗糖垫结合,原理是先除去非囊泡物质,再通过梯度密度浓缩提取外泌体,该方法可以得到相对较为纯净的外泌体。传统的梯度密度方法通常需要离心16h,但是2012年,研究者[15]使用了62~90h才分离出某些确切囊泡,因此,该方法可能不足以沉淀所有的外泌体。如果离心时间不充足,污染物质可能和外泌体保持在相同的密度层,特别是这个密度范围又比较宽。外泌体的提取方法:磁珠免疫法。宁波外泌体提取试剂进货价
外泌体提取:使用抗体包被珠子的分离不适合从大量样本中获得外泌体。厦门外泌体提取试剂推荐厂家
1996年GRaposo等发现类似于B淋巴细胞的免疫细胞也会分泌抗原呈递外泌体(antigenpresentingvesicle),所分泌的外泌体可以直接刺激效应CD4+细胞的抗一些病症反应。2007年HValadi等进一步发现细胞之间可以通过外泌体中RNA交换遗传物质。随着有关外泌体研究越来越多,研究者发现它普遍参与了机体免疫应答、抗原呈递、细胞分化、一些病症生长于侵袭等各种生物过程中。目前的主流观点认为,外泌体的产生过程为:细胞膜内陷,形成内体(endosome),再形成多泡体(multivesicularbodies,MVB),较后分泌到胞外成为外泌体。外泌体中携带有母细胞的多种蛋白质、脂类、DNA和RNA等重要信息。外泌体较早见于1981年,EGTrams等在体外培养的绵羊红细胞上清液中发现了有膜结构的小囊泡,并命名为exosome。对于外泌体的作用,当时推测为细胞排泄废物的一种方式。厦门外泌体提取试剂推荐厂家
外泌体的提取方法:1.超速离心法(差速离心)。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。2.密度梯度离心。在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。有的是通过特殊设计的过滤器过滤掉杂质成分,有的...
- 昆明正规外泌体提取试剂哪里买 2025-12-28
- 北京外泌体提取试剂服务电话 2025-12-28
- 南昌外泌体提取试剂销售厂家 2025-12-28
- 广州外泌体提取试剂单价 2025-12-27
- 广州正规外泌体提取试剂直销价 2025-12-27
- 合肥正规外泌体提取试剂推荐厂家 2025-12-27
- 济南外泌体提取试剂服务电话 2025-12-27
- 广州外泌体提取试剂厂家直销 2025-12-27
- 上海正规外泌体提取试剂产品介绍 2025-12-26
- 南京外泌体提取试剂厂家供应 2025-12-26
- 郑州外泌体提取试剂供应商 2025-12-25
- 成都外泌体提取试剂进货价 2025-12-25
- 合肥正规外泌体提取试剂单价 2025-12-25
- 太原正规外泌体提取试剂推荐厂家 2025-12-24
- 上海正规外泌体提取试剂哪里买 2025-12-24
- 南京外泌体提取试剂单价 2025-12-24


- 成都正规细胞高效转染试剂厂家推荐 12-30
- 重庆细胞高效转染试剂服务电话 12-30
- 南京细胞高效转染试剂哪家便宜 12-30
- 芜湖正规细胞高效转染试剂进货价 12-30
- 长沙细胞高效转染试剂服务电话 12-30
- 济南细胞高效转染试剂产品介绍 12-30
- 宁波细胞高效转染试剂推荐厂家 12-30
- 唐山正规细胞高效转染试剂哪家好 12-30
- 芜湖深圳细胞高效转染试剂 12-30
- 徐州正规细胞高效转染试剂推荐厂家 12-30





