- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体在肺病治病中的作用:有研究表明,一些病症来源的外泌体对一些病症免疫的调控具有一定的影响作用,包括免疫压制和免疫启动两个方面。Romagnoli等研究发现,肺病细胞可以刺激树突状细胞等抗原提呈细胞产生携带特异性的病抗原的外泌体,这些外泌体可以迁移到区域淋巴结,进而启动CD4+T与CD8+T细胞产生抗一些病症免疫反应,进而压制一些病症生长。Besse等研究发现,在晚期NSCLC患者中,装载有IFN-γ,MHCI和MHCⅡ限制性的病抗原的树突状细胞外泌体增强了NK细胞的抗一些病症免疫功能,研究证实外泌体参与相关一些病症生理病理过程,在NSCLC免疫治病中有着重要的临床应用价值,为NSCLC的治病打开了新的视野。同时可获得高纯度和高回收率的外泌体——如新西兰IZON开发的系列的外泌体排阻剂。重庆正规外泌体提取试剂

外泌体相关miRNA与肺病的诊断:进一步研究发现,另外6种外泌体(miR-151a-5p、-30a-3p、-200b-5p、-629、-100、-154-3p)可用于肺病的诊断,其AUC为0.76。这些miRNAs具有NSCLC早期诊断的高度敏感性,有望成为NSCLC早期诊断筛查的生物标志物。在临床应用方面,目前ExosomeDiagnostics公司研发的基于血浆外泌体的ALK试剂盒已于2016年初被美国FDA批准用于临床。这是世界上个以血液样本分析外泌体RNA的临床液体活检。这项方法可以准确、实时地检测NSCLC患者的EML4-ALK突变,通过比较NSCLC患者组织ALK水平和相应的血浆样本发现该项检测可以达到88%的诊断灵敏度和100%的诊断特异性。而此前,对于EML4-ALK的检测是基于组织活检的FISH或IHC,而且,FISH缺乏灵敏性,误诊率也较高。济南外泌体提取试剂单价超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。

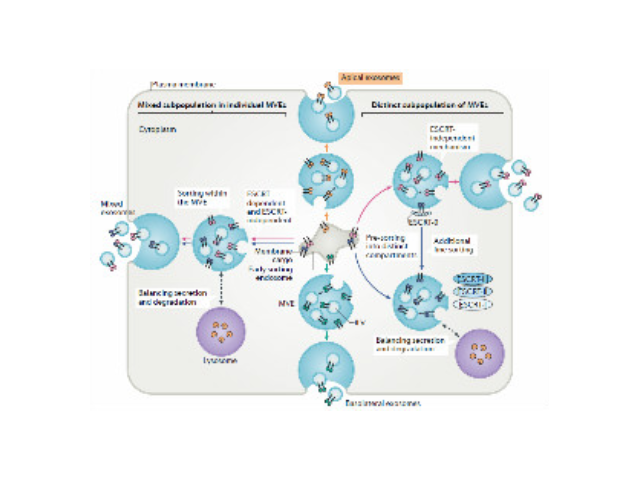
多泡内体的腔内囊泡,要么分选进溶酶体将物质降解,要么作为外泌体分泌到胞外环境中。将膜分选到不同的腔内囊泡群中的机制尚不清楚。该研究发现物质被分选到内体膜上的不同子域中,并且外泌体相关结构域向内体腔的转移不取决于ESCRT(运输所需的内体分选复合体)的功能,但是需要鞘脂神经酰胺。纯化的外体富含神经酰胺,并且在神经鞘磷脂酶被压制后外泌体释放减少。这些结果确定了内体内膜运输和外泌体形成的途径。环-GMP-AMP合酶(cGAS)在细菌传染期间检测胞质DNA并诱导抗细菌状态。cGAS信号通过合成第二信使——环GMP-AMP(cGAMP),启动干扰素基因的刺激物(STING)。该研究表明,当它们在cGAS表达细胞中产生时,cGAMP被整合到细菌颗粒中,包括慢细菌和疱疹细菌颗粒。细菌体将cGAMP转移至新传染的细胞并引发STING依赖性抗细菌程序。这些效应**于外泌体和细菌核酸。研究结果揭示了天然免疫信号在细胞间转移的途径,可能加速和扩大抗细菌反应。此外,用装载cGAMP的慢细菌传染树突细胞增强了它们的活化。因此,用cGAMP加载细菌载体对于疫苗开发具有很大希望。
研究探讨了外泌体是否可以作为RNAi的有效载体的可能性。与脂质体和其他合成药物纳米颗粒载体不同,外泌体含有可能增强内吞作用的跨膜和膜锚定蛋白,从而促进其内容物的递送。CD47是外泌体蛋白质之一,是一个普遍表达的整合素相关跨膜蛋白,其部分功能可以保护细胞免受吞噬作用。CD47是信号调节蛋白α(SIRPα,也称为CD172a)的配体,CD47-SIRPα间的结合能够发出“不要吃我”的信号,从而压制吞噬作用。病基因RAS能够促进胰腺病细胞增殖,增强胞饮作用从而促进一些病症细胞摄取外泌体。合成纳米颗粒对细胞有一定毒性作用,但使用外泌体能够较小化对细胞的毒性。研究人员发现,CD47和病基因KRAS驱动的胞饮作用都会压制外泌体被循环系统的清理,并增强胰腺病细胞对外泌体的特异性。所以,外泌体的这种特性增强了它们通过递送RNAi来特异性靶向胰腺病中的KRAS的能力,并且使用外泌体作为单一靶向剂显着改善了所有实验PDAC小鼠模型的总生存期。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀。

研究初次发现疟原虫传染小鼠血浆外泌体(exosomes)能够压制一些病症血管生成,并初步阐明其分子机制。研究加深了对疟原虫传染宿主所分泌的外泌体与一些病症血管生成之间的相互作用的认识,为开发疟原虫传染来源的外泌体作为一种新型抗一些病症制剂奠定了基础。研究人员选用肺病小鼠模型作为研究对象,从传染疟原虫的小鼠血浆中获得外泌体,并将这些外泌体注射到小鼠的一些病症内部,并与没有疟原虫传染的小鼠血浆外泌体进行对照。研究发现,疟原虫传染小鼠的血浆外泌体明显压制一些病症血管的生成。进一步的研究发现,疟原虫传染的小鼠血浆外泌体通过至少四种特殊的微小RNA(miR16-5p/17-5p/322-5p/497-5p)压制血管内皮细胞VEGF受体(VEGFR2)的表达从而阻断血管生成的信号通路。这些发现加深了人们对疟原虫抗病机理的理解,并为疟原虫疗法治病一些疾病的临床研究提供进一步的理论依据。将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层。宁波正规外泌体提取试剂供应商
可将外泌体吸附并分离出来。重庆正规外泌体提取试剂
外泌体作为RNAi药物载体的疗效:这项研究,检测了利用exosomes作为RNAi靶向药物的效果,并证明了这个过程中exosomes进行免疫逃逸的机制:对exosomes进行基因修饰(命名为iExosome),装载上靶向胰腺病细胞KRAS突变基因的RNA干扰药物,在小鼠模型上进行试验,结果表明,iExosome比同样经过修饰的脂质iLiposome递送效果更好,能够压制侵袭性胰腺病生长;这得益于exosomes表面的CD47,它能够阻止exosomes在血液循环系统中被单核细胞清理。这项研究结果对致力于exosomes转化医学的科学家来说,可谓振奋人心!重庆正规外泌体提取试剂
苏州君欣生物科技有限公司是一家苏州君欣生物科技有限公司的经营范围包括原代细胞的定制以及相关产品的配套销售与服务,干细胞染色体核型分析与鉴定、无血清细胞培养基以及无血清细胞冻存等系列产品的生产与销售,动物疾病模型的构建以及药物效果的验证等领域。的公司,是一家集研发、设计、生产和销售为一体的专业化公司。苏州君欣生物科技拥有一支经验丰富、技术创新的专业研发团队,以高度的专注和执着为客户提供原代细胞,无血清细胞冻存液,干细胞无血清培养基,动物疾病模型。苏州君欣生物科技始终以本分踏实的精神和必胜的信念,影响并带动团队取得成功。苏州君欣生物科技始终关注精细化学品市场,以敏锐的市场洞察力,实现与客户的成长共赢。
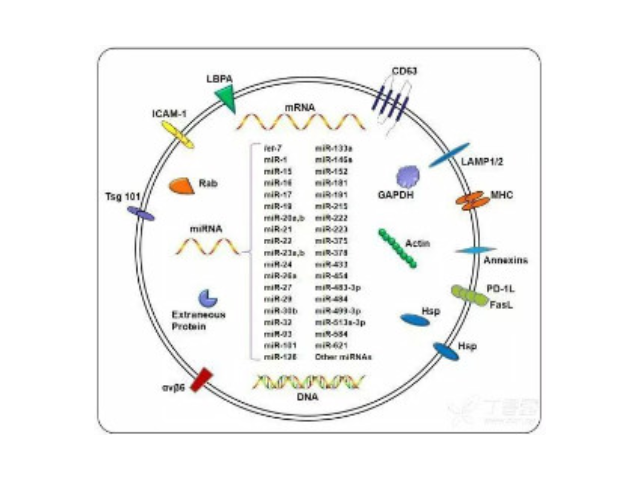
外泌体(Exosome)是由细胞分泌而来的微小囊泡,直径约为30-200nm,密度在1.13-1.21g/ml,具有杯状形态、双层膜结构,天然存在于血液、尿液、唾液、母乳和细胞培养基等生物体液中。包括瘤细胞在内几乎所有类型的细胞(免疫细胞、神经细胞、干细胞),都可以产生并释放exosome。Exosome内含有与细胞来源相关的蛋白质rRNA和microRNA,Exosome可通过细胞膜受体直接受体细胞,也可运输蛋白质、mRNA、miRNA、lncRNA、circRNA,甚至细胞器进入受体细胞,参与细胞间通讯。Exosome在免疫应答、炎症反应、血管生成、凋亡、凝血和废物处理等生理过程发挥关键作...
- 石家庄正规外泌体提取试剂厂家供应 2026-05-19
- 厦门外泌体提取试剂哪家好 2026-05-19
- 合肥正规外泌体提取试剂价格 2026-05-17
- 温州外泌体提取试剂直销厂家 2026-05-17
- 长沙外泌体提取试剂平均价格 2026-05-17
- 芜湖外泌体提取试剂单价 2026-05-16
- 芜湖外泌体提取试剂哪家便宜 2026-05-16
- 重庆外泌体提取试剂报价 2026-05-16
- 石家庄外泌体提取试剂厂家供应 2026-05-15
- 昆明正规外泌体提取试剂直销厂家 2026-05-15
- 南昌外泌体提取试剂单价 2026-05-14
- 唐山外泌体提取试剂厂家 2026-05-14
- 无锡正规外泌体提取试剂哪家便宜 2026-05-14
- 南京外泌体提取试剂厂家直销 2026-05-13
- 温州正规外泌体提取试剂推荐厂家 2026-05-13
- 贵阳外泌体提取试剂哪家好 2026-05-13


- 杭州正规细胞高效转染试剂单价 05-19
- 青岛无血清细胞冻存液报价 05-19
- 郑州正规无血清细胞冻存液哪家便宜 05-19
- 浙江糖原染色试剂盒直销价 05-19
- 长沙正规RNA提取试剂生产厂家 05-19
- 正规细胞外基质胶价格 05-19
- 武汉正规无血清细胞冻存液推荐厂家 05-19
- 无锡外泌体提取试剂哪家好 05-19
- 山东咨询糖原染色试剂盒产品介绍 05-19
- 贵阳RNA提取试剂厂家供应 05-19