传统的药物组合筛选方法主要包括基于细胞实验的筛选和动物模型筛选。基于细胞实验的筛选是在体外培养的细胞系中,将不同药物以不同浓度组合添加,通过检测细胞的生长、增殖、凋亡等指标,评估药物组合的效果。这种方法操作相对简单、成本较低,能够在较短时间内对大量药物组合进行初步筛选。例如,通过 MTT 法、CCK-8 法等检测细胞活性,判断药物组合对细胞的抑制或促进作用。动物模型筛选则是将药物组合应用于实验动物,如小鼠、大鼠等,观察药物组合在体内的医疗效果和安全性。动物模型更接近人体生理环境,能够反映药物在体内的代谢、分布等情况,为药物组合的有效性和安全性提供更可靠的依据。但动物模型筛选成本高、周期长,且存在种属差异,实验结果不能完全准确地预测在人体中的效果。传统方法虽然在药物组合筛选中发挥了重要作用,但在面对海量药物组合时,其效率和准确性有待提高。基于类organ技术,环特生物升级药物筛选体系,贴近人体生理状态。蛋白抑制剂药物筛选

“橘生淮南则为橘,生于淮北则为枳”,这句古语生动地说明了产地环境对药材品质的重要影响。不同的地理气候条件,如土壤、光照、温度、水分等,会赋予药材独特的化学成分和药物的性能。例如,道地药材人参主要产于东北的长白山地区,那里气候寒冷、土壤肥沃,人参在生长过程中积累了丰富的人参皂苷等有效成分,具有大补元气、复脉固脱等功效,品质优良。而其他地区种植的人参,由于产地环境不同,其化学成分和药物的性能也会有所差异,质量相对较差。因此,在原料药材筛选过程中,产地环境是一个关键因素。科研人员会通过对不同产地药材的化学成分分析、药效学研究等,确定质量药材的产地范围和生态环境特征。同时,为了保护和传承道地药材,还会采取一系列措施,如建立道地药材生产基地、加强产地环境监测等,确保药材的品质和特色。只有充分考虑产地环境的影响,才能筛选出具有优良品质的原料药材,为中医药的疗效提供保障。筛选化合物环特生物的药物筛选服务支持 “蓝帽” 备案,适配保健食品研发。
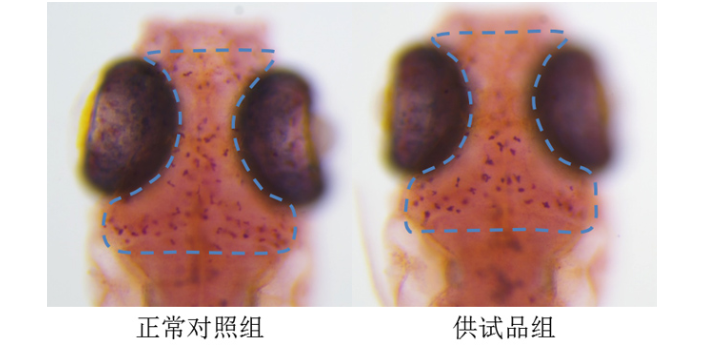
罕见病由于患者数量少、市场需求小,长期以来面临着药物研发困境。环特药物筛选为罕见病药物研发带来了新的希望。利用斑马鱼模型,可以模拟多种罕见病的病理特征,为药物筛选提供有效的实验平台。例如,对于一些遗传性罕见病,通过基因编辑技术在斑马鱼中引入相应的基因突变,构建疾病模型。然后,将大量的化合物库应用于这些模型斑马鱼,筛选出能够改善疾病症状或纠正病理变化的潜在药物。由于斑马鱼实验的高效性,能够在较短时间内对大量化合物进行筛选,很大增加了发现罕见病医疗药物的机会。环特药物筛选为罕见病患者带来了更多医疗的可能,推动了罕见病药物研发领域的进步。
筛药实验(DrugScreening)是药物研发的初始阶段,旨在从大量化合物中快速筛选出具有潜在活性的候选药物。这一过程通过高通量技术,对化合物库中的分子进行系统测试,评估其对特定靶点(如酶、受体)的抑制能力。其主要价值在于大幅缩小研究范围,将资源聚焦于有前景的分子,避免盲目研发带来的时间和成本浪费。例如,抗ancer药物研发中,筛药实验可快速识别出能抑制肿瘤细胞增殖的化合物,为后续临床前研究奠定基础。此外,筛药实验还能发现新作用机制的药物,为医疗耐药性疾病提供新策略。随着人工智能和自动化技术的发展,现代筛药实验的效率和准确性明显提升,成为药物创新的关键驱动力。罕见病药物筛选难度大,环特生物定制化模型解除解研发痛点。

高通量组学技术(如基因组、转录组、蛋白质组)为耐药机制研究提供了系统视角。全基因组测序(WGS)可多方面解析耐药株的突变图谱。例如,对多重耐药结核分枝杆菌的WGS分析发现,rpoB、katG和inhA基因突变分别导致利福平、异烟肼和乙胺丁醇耐药,且突变株在群体中的传播速度明显快于敏感株。转录组学(RNA-seq)则揭示耐药相关的基因表达调控网络。例如,在伊马替尼耐药的慢性髓系白血病细胞中,RNA-seq发现BCR-ABL下游信号通路(如PI3K/AKT、RAS/MAPK)异常开启,且药物外排泵(如ABCB1)表达上调。蛋白质组学(质谱技术)可鉴定耐药相关的蛋白修饰变化。例如,在顺铂耐药的卵巢ancer细胞中,质谱分析发现铜转运蛋白ATP7B表达升高,其通过将顺铂泵出细胞外降低胞内药物浓度,为联合使用铜螯合剂逆转耐药提供了依据。针对特定疾病的药物筛选,要深入了解疾病的发病机制。组合药物筛选
药物筛选的阳性对照设置合理,能准确判断化合物的活性。蛋白抑制剂药物筛选
体外筛选是耐药株研究的基础手段,主要包括药物浓度梯度法、间歇给药法和自适应进化法。浓度梯度法通过将病原体暴露于递增药物浓度中,筛选存活株并测定小抑菌浓度(MIC)。例如,在耐药菌筛选中,将大肠杆菌置于含亚抑制浓度头孢曲松的培养基中,每48小时转接至更高浓度,持续30天后获得MIC提升16倍的耐药株。技术优化方面,微流控芯片结合荧光标记技术可实现单细胞水平的耐药株动态监测。例如,通过微流控装置捕获单个肿瘤细胞,实时观察其对吉非替尼的响应,发现EGFRT790M突变株在药物处理后存活率高于野生型。此外,CRISPR/Cas9基因编辑技术可定向构建耐药相关基因突变株,加速机制解析。例如,在慢性髓系白血病细胞中敲入BCR-ABLT315I突变,模拟伊马替尼耐药表型,为第二代酪氨酸激酶抑制剂研发提供模型。蛋白抑制剂药物筛选