根据模板设计,无细胞蛋白表达技术可分为线性模板和环状模板表达。线性模板(如PCR产物)无需克隆,快速启动表达,但稳定性差、产量较低,适用于Batch体系的快速筛选。环状模板(如质粒DNA)通过克隆技术制备,稳定性高且产量提升,适合CECF体系的大规模生产(如抗体或抗原制备)。此外,结合T7/T3/SP6启动子的偶联转录/翻译系统(如TNT系统)可直接以DNA为模板,简化流程并提高效率。以上形式可根据需求组合使用,例如原核CECF系统+环状模板用于工业化生产,或真核Batch系统+线性模板用于快速筛选。添加0.5 mM镁离子可优化小麦胚芽体外蛋白表达的翻译起始效率。大肠杆菌诱导蛋白表达产业链

20世纪90年代后,随着分子生物学和合成生物学的进步,无细胞蛋白表达技术技术迎来突破。研究者通过优化裂解物制备(如敲除大肠杆菌核酸酶)、开发能量再生系统(如Phosphoenolpyruvic acid,PEP循环),明显提升蛋白产量和反应时长。2000年代初,连续交换式反应体系(CECF)的出现解决了底物耗尽问题,使反应时间延长至24小时以上,产量达毫克级,为工业化铺平道路。此阶段,无细胞蛋白表达技术开始应用于毒性蛋白合成和抗体片段生产,但成本仍较高。iptg诱导蛋白表达修饰大肠杆菌裂解物添加含T7启动子的线性DNA后,裂解物中的内源性RNA聚合酶即可转录mRNA。
凋亡因子(如caspase-3)、细菌du su(如白喉du suA链)在细胞内表达会引发宿主死亡。体外蛋白表达系统通过无细胞环境规避毒性效应:在添加线粒体膜组分的兔网织红细胞裂解物中,全长BAX蛋白(21kDa)表达量达0.8mg/mL,并成功模拟其介导的细胞色素C释放过程(CellDeathDiffer.,2024)。该系统还可表达HIV蛋白酶(活性>95%),用于高通量抑制剂筛选,加速抗病毒药物开发。真he dan白的糖基化修饰(如抗体Fc段N-糖)是zhi liao性蛋白功能的he xin。传统体外蛋白表达因缺乏高尔基体,糖基化效率不足5%。突破性方案是在HEK293裂解物中添加重组糖基转移酶复合体(含GnT-I、GnT-II、FUT8),使曲妥珠单抗的复杂双触角糖型比例升至80%(Science,2022)。结合UDP-GlcNAc底物连续补料,糖均一性(G0F:G2F=1:1.2)媲美哺乳细胞表达,为下一代抗体偶联药物(ADC)提供新生产路径。
体外蛋白表达正在革新现场快速检测技术。以疟疾诊断为例:将冻干的大肠杆菌裂解物、疟原虫 HRP2 基因 DNA 及显色底物预装在微流控芯片中,加入水样后启动 30 分钟体外蛋白表达反应,生成的 HRP2 蛋白催化显色剂变红,灵敏度达 5 寄生虫/μL(传统试纸只 200/μL)。此方案在刚果金野外测试中显示,阳性检出率提升 40% 且无需冷链运输。类似技术已扩展至COVID-19检测——用患者鼻拭子 RNA 直接合成 Spike 蛋白,结合纳米金抗体实现 1 小时确诊。这种 “即测即表达”模式 将诊断成本降至 $0.5/次,成为资源匮乏地区的抗疫利器。在冰上预混裂解物与能量混合物,是保证体外蛋白表达重复性的关键步骤。

相较于原核表达体系,真核体外蛋白表达的he xin优势在于具备部分翻译后修饰能力,但 关键修饰途径仍存在明显局限。在缺乏内质网-高尔基体转运机制的情况下,糖基化修饰通常终止于高甘露糖型(Man₅GlcNAc₂)阶段,无法合成复杂双触角唾液酸化糖链。这一缺陷直接影响zhi liao性抗体的抗体依赖性细胞介导的细胞毒性(ADCC)效应。同时,裂解物中二硫键异构酶(PDI)与分子伴侣(如BiP)的活性不足,导致含多对二硫键的蛋白错误折叠率升高40%-60%。为克服此瓶颈,需在裂解物中外源性添加重组糖基转移酶复合体(如GnT-I/GnT-II/FUT8)以重构修饰途径,并通过优化氧化还原电势(Eh=-230 mV至-280 mV)改善二硫键形成效率。体外蛋白表达的这些修饰缺陷是目前制约其应用于功能性糖蛋白生产的主要因素。添加 0.1% Triton X-100 使疏水蛋白的体外表达可溶率达90%。目的蛋白表达水平
当体外蛋白表达效率不足时,需检测模板完整性并优化启动子强度。大肠杆菌诱导蛋白表达产业链
在合成生物学中,无细胞蛋白表达技术是构建人工细胞和基因电路的he xin工具。研究人员通过混合不同物种(如大肠杆菌+哺乳动物)的裂解物,创建杂合翻译系统,以实现跨物种蛋白的协同合成。该技术还支持无细胞基因线路的快速原型设计,例如将CRISPR组分与报告蛋白共表达,用于体外诊断工具的开发。由于摆脱了细胞膜的限制,CFPS可直接整合非生物元件(如合成聚合物或纳米材料),推动人工合成生命和生物-非生物杂合系统的前沿研究。无细胞蛋白表达技术可快速表达膜蛋白(如GPCRs、离子通道)用于药物靶点研究,解决了此类蛋白在细胞内难表达、易沉淀的问题。在诊断领域,基于CFPS的体外转录-翻译系统被整合到便携式设备中,用于现场检测病原体核酸(如埃博拉病毒),实现“样本进-结果出”的快速诊断。此外,该技术还能合成定制化抗原,用于抗体库筛选或个性化cancer疫苗开发。大肠杆菌诱导蛋白表达产业链
传统的蛋白质表达纯化流程极其依赖人工操作,并且往往需要几周或者几个月的时间.无细胞蛋白表达的兴起可将...
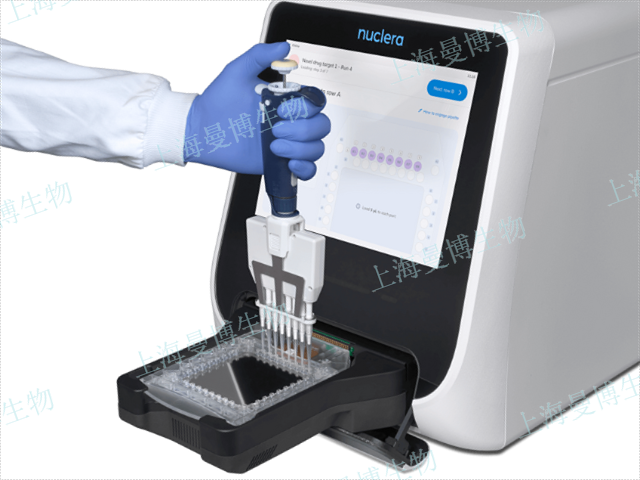
【详情】eProtein Discovery系统:一种将无细胞蛋白合成与数字微流控相结合的快速蛋白质原型...
【详情】无细胞蛋白表达的兴起可将这一时间缩短至十几个小时,但是仍需要现进行表达载体的制备,体外扩增和高通量蛋...
【详情】体外蛋白表达已成为生物学教学的高效工具。高中生使用 “GFP 荧光蛋白表达试剂盒”(含冻干裂解物和 ...
【详情】尽管体外蛋白表达在科研领域优势明显,其规模化应用仍面临三重挑战:裂解物制备成本高: 真核裂解物(如兔...
【详情】体外蛋白表达系统的明显缺陷在于 缺乏真核细胞器结构,导致关键翻译后修饰难以实现:糖基化不完整性: 裂...
【详情】若需实现高阶应用(如非天然氨基酸插入、膜蛋白合成),无细胞蛋白表达技术复杂度会明显提升。例如,插入A...
【详情】相较于原核表达体系,真核体外蛋白表达的he xin优势在于具备部分翻译后修饰能力,但 关键修饰途径仍...
【详情】尽管前景广阔,无细胞蛋白表达技术市场仍面临成本控制和规模化生产的挑战。目前反应体系依赖昂贵的裂解物和...
【详情】