- 品牌
- MCE,艾德莱,OriGene,abmart,ABW基质胶
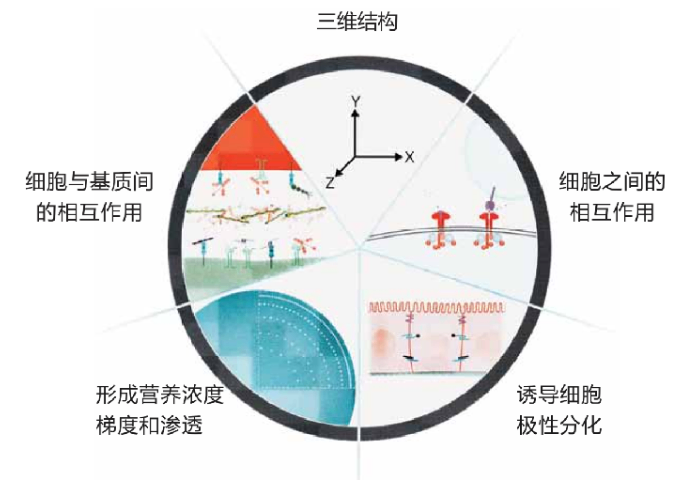
基质胶(Matrigel)是一种从小鼠**中提取的细胞外基质(ECM)成分,主要由胶原蛋白、层粘连蛋白、糖胺聚糖等组成。它为细胞提供了一个三维的生长环境,模拟了体内的微环境,促进细胞的附着、增殖和分化。在类***培养中,基质胶的使用至关重要,因为它不仅为细胞提供了结构支持,还能通过与细胞表面的受体相互作用,***多种信号通路,促进细胞的生长和功能表现。基质胶的成分和物理特性使其成为研究细胞行为、组织再生和疾病模型的重要工具,尤其是在**生物学和干细胞研究领域。类器官在基质胶中的尺寸需定期监测以避免中心坏死。建德低细胞凋亡率基质胶-类器官培养性价比高

基质胶不仅为细胞提供支撑,还通过细胞间的相互作用影响类***的形成和功能。细胞在基质胶中的生长和分化受到基质成分、结构和力学特性的影响。细胞通过细胞膜上的整合素与基质胶结合,***细胞内的信号通路,进而调节基因表达和细胞行为。此外,细胞间的相互作用也会影响类***的形态和功能。例如,细胞间的信号传递可以促进细胞的聚集和组织形成,从而提高类***的复杂性和功能。因此,深入研究基质胶与细胞间的相互作用,对于优化类***培养和提高其生物学功能具有重要意义。建德模基生物基质胶-类器官培养实验步骤基质胶为类器官提供仿生微环境,促进三维结构形成。
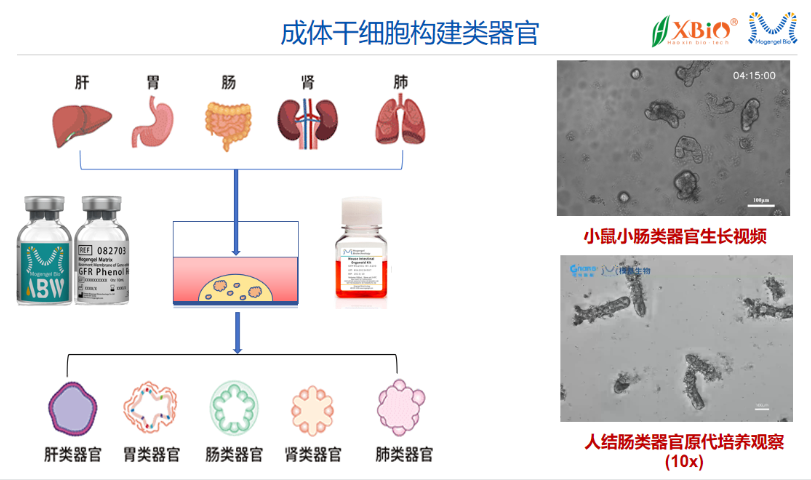
基质胶-类器官培养技术在生物医学研究中展现出广阔的前景。未来,随着基因编辑技术、单细胞测序技术等的进步,类***的研究将更加深入。研究人员可以利用这些技术对类***进行更为精细的调控,探索细胞间的相互作用和信号传导机制。此外,基质胶的改良和新型生物材料的开发也将推动类***技术的发展,使其在药物筛选、疾病模型建立和再生医学等领域的应用更加***。总之,基质胶-类器官培养技术将为我们理解生命过程和疾病机制提供新的视角和工具。
尽管基质胶类***技术取得***进展,仍面临若干关键挑战。标准化问题是首要障碍,不同批次的天然基质胶存在***差异,影响实验可重复性。复杂类***模型的构建仍需突破,如具有完整免疫微环境的类***培养仍然困难。规模化生产面临成本和技术双重挑战,特别是临床级类***的培养要求。未来发展方向包括:开发化学成分明确的标准基质胶替代品;结合3D生物打印技术实现类***的精细构建;发展智能响应性材料模拟动态微环境变化;建立自动化培养和质量控制体系。随着材料科学、干细胞技术和生物工程的交叉融合,基质胶类***技术有望在疾病建模、药物开发和再生医学等领域发挥更大作用。特别值得关注的是器官芯片技术的发展,将为基质胶类***提供更接近体内的培养环境。类器官与基质胶的RNA测序需同步分析ECM相关基因。

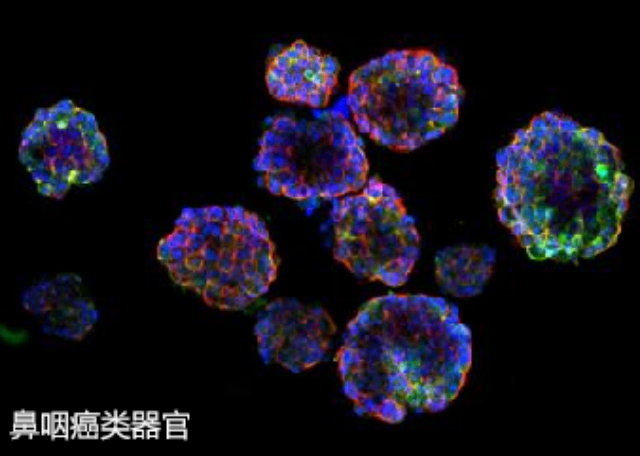
基质胶培养的类***为疾病研究提供了**性的模型系统。在**研究领域,患者来源类***(PDOs)保留原发**的组织结构和分子特征,已成为个性化医疗的重要工具。通过调节基质胶的硬度可以模拟不同阶段的**微环境,如较硬的基质(~8kPa)可诱导乳腺*的侵袭表型。在遗传性疾病研究中,囊性纤维化类***模型可以重现CFTR基因突变导致的病理变化。***进展是将基质胶类***与微流控系统结合,构建包含血管网络的复杂疾病模型,这为研究**转移和药物渗透提供了更真实的平台。此外,基质胶的组成调控还可以模拟特定病理条件下的ECM重塑,如肝纤维化中胶原沉积的增加。基质胶的弹性模量调控类器官的干性维持或分化倾向。临平区模基生物基质胶-类器官培养怎么试用
类器官在基质胶中的自发凋亡可能提示生长因子缺乏。建德低细胞凋亡率基质胶-类器官培养性价比高
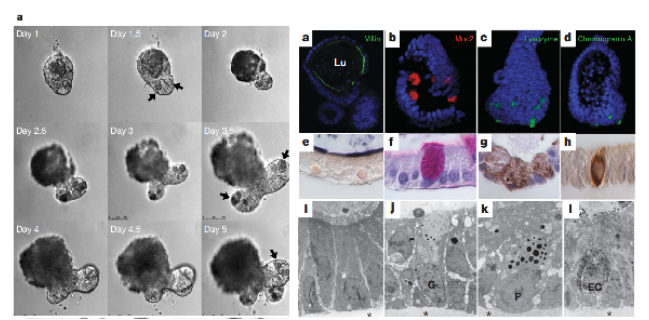
类***的生长依赖基质胶与生长因子的协同作用。例如,肠类***需要Wnt3a、EGF和Noggin嵌入基质胶中以***Lgr5+干细胞增殖;而脑类***需FGF2和Sonic Hedgehog梯度诱导神经分化。基质胶的缓释特性可稳定生长因子活性,避免频繁补料。研究显示,将VEGF共价偶联至巯基化透明质酸胶中,能延长血管类***的成型时间。优化生长因子-基质胶组合(如浓度、时空释放)是提高类***模拟疾病或发育过程的关键。基质胶的弹性模量(通常0.5-5kPa)直接调控类***的形态发生。软胶(<1kPa)促进乳腺类***的导管分支,而硬胶(>3kPa)更利于肝*类***的致密团簇形成。通过动态调整胶硬度(如光响应水凝胶),可模拟纤维化或**微环境的力学变化。此外,胶的孔隙率影响营养渗透和类***大小,高孔隙海藻酸盐胶能支持更大规模的胰岛类***培养。结合微流控技术,可实现在单芯片中多硬度区域的并行测试。建德低细胞凋亡率基质胶-类器官培养性价比高
- 温州基质胶-类器官培养多少钱 2026-05-03
- 衢州基质胶-类器官培养卖价 2026-05-03
- 余杭区模基生物基质胶-类器官培养怎么试用 2026-05-03
- 西湖区高成功率基质胶-类器官培养性价比高 2026-04-29
- 临安区ABW基质胶-类器官培养价格怎么样 2026-04-28
- 富阳区高成功率基质胶-类器官培养 2026-04-28
- 浙江基质胶-类器官培养报价 2026-04-28
- 拱墅区肿瘤基质胶-类器官培养价格怎么样 2026-04-27