Itrytoexplainwhytwo-photonmicroscopyhasadeeperimagingdepththanone-photonmicroscopy,intheareaofbiomedicalimaging.Manyofthebiomedicalimagingmodalities,nomatterone-photon(confocal)ormulti-photon(two-photon),uselasersaslightsourceandrequirecompatiblefluorescentdyes.Fluorescentdyeshavetheirownexcitationwavelength,andtheycaneitherbeexcitedbyasinglephotonwiththephotonenergyofthatexcitationwavelength(E=hv=h*c/λ);orbytwophotons,arrivingalmostatthesametime,buteachwithapproximatelyhalfoftheenergy,henceofdoublewavelengththanone-photon(0.5E->2λ).Theformeristheprincipleofone-photonmicroscopyandthelatteristheprincipleoftwo-photonmicroscopy.Whenimagingthesamefluorescentdye,sincetwo-photoncoulduseapproximatelydoubledwavelengthcomparedwithsingle-photon,two-photoncanobviouslypenetrateddeeperintothetissueduetolessscattering(longerwavelength,lessscattering).双光子显微镜使用的是可见光或近红外光作为光源。布鲁克双光子显微镜成像原理

2008年钱永健等人由于荧光蛋白(GFP,绿色荧光蛋白)的发现和使用,获得了诺贝尔化学奖,是对荧光成像技术的一次巨大肯定和推动。与荧光蛋白以及荧光染料等标记物在细胞中的定位与表达技术相结合,使得科学家可以特异性的分辨生物体乃至细胞内部不同结构与成分,并且能够在生命体和细胞仍具有活性的状态下(状态)对其功能进行动态观察。这就使得荧光成像技术成为了无可替代的,生物学家现今较为重要的技术手段之一。目前,大多数细胞生物学和生理学研究主要还是在离体培养的细胞体系中研究。然而与细胞生物学研究有所不同的是,大脑的功能研究的整体性和原位性显得更加关键:只研究分离的神经元无法解释神经系统的功能和规律。由于被观测的信号会受到样本组织的散射和吸收,根本无法穿透如此深的组织进行成像。而双光子显微镜(Two-photonMicroscopy,简称TPM)的发明,则为此类研究带来了希望。国内双光子显微镜厂家由于双光子显微镜使用的是可见光或近红外光作为激发光源,适用于长时间的研究。
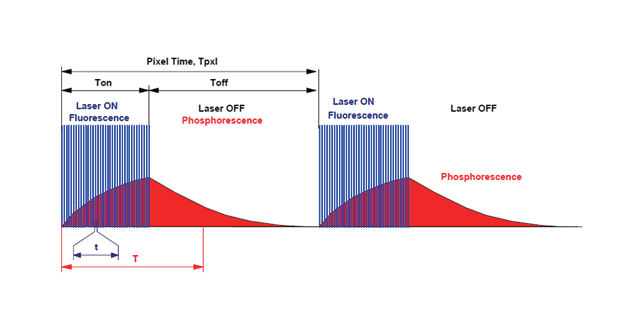
高光子密度带来的高能量容易损伤细胞,所以双光子显微镜使用高能量锁模脉冲激光器。这种激光器发出的激光具有很高的峰值能量和很低的平均能量,其脉冲达到最大值所持续的周期只有十万亿分之一秒,而其频率可以达到80至100兆赫,这样即能达到双光子激发的高光子密度要求,又能不损伤细胞,使扫描能更好地进行。双光子显微镜在各领域研究中已有许多成功实例生物领域:贝尔实验室的Svoboda等人研究了大脑皮层神经元细胞内钙离子动力学情形。利用双光子显微镜观察到的现象证明了钙离子的增加依赖于肌体触发的钠离子作用电势。信息领域:美国科学家Rentzepis提出了一种在现有二维光盘的基础上将数据储存扩展到三维空间。由于双光子激发具有作用精细体积小的特点,避免了层与层之间的互相干扰,极大地提高了数据储存密度。
双光子荧光显微镜是激光扫描共聚焦显微镜和双光子激发技术相结合的新技术。双光子激发的基本原理是:在光子密度较高的情况下,荧光分子可以同时吸收两个波长较长的光子,经过短暂的所谓激发态寿命后,发射一个波长较短的光子;效果和用波长为长波长一半的光子激发荧光分子是一样的。双(多)光子成像的优点是具有更深的组织穿透深度,红外光可以在平面上探测到极限为1mm的组织区域;因为信号背景比高,所以具有更高的对比度;由于激发体积小,具有定点激发、光毒性小的特点;激发波长由紫外、可见光调整为红外激发,更加安全。双光子显微镜在各领域研究中已有许多成功实例。

双光子显微镜(2PM)可以对钙离子传感器和谷氨酸传感器进行亚细胞分辨率的成像,从而测量不透明脑深部的活动。成像膜的电压变化可以直接反映神经元的活动,但神经元活动的速度对于常规的2PM来说太快了。目前,电压成像主要由宽视场显微镜实现,但其空间分辨率较差,且只能在浅深度成像。因此,为了以高空间分辨率成像不透明脑中膜电压的变化,需要将成像速率提高2PM。面向模块输出端的子脉冲序列可视为从虚拟光源阵列发出的光,这些子脉冲在中继到显微镜物镜后形成空间分离和时间延迟的聚焦阵列。然后,该模块被集成到一个带有高速数据采集系统的标准双光子荧光显微镜中,如图2所示。光源是重复频率为1MHz的920nm激光器。FACED模块可以产生80个脉冲焦点,脉冲时间间隔为2ns。这些焦点是虚拟源的图像。虚光源越远,物镜处的光束尺寸越大,焦点越小。光束可以沿Y轴比沿X轴更好地填充物镜,从而在X轴上产生0.82m和0.35m的横向分辨率。双光子显微镜在组织透明化成像中应用。bruker双光子显微镜商家
双光子显微镜可以在小鼠的的任何部位进行有生命体成像。布鲁克双光子显微镜成像原理
目前,世界各国的脑科学研究如火如荼,中国的脑计划也即将启动。其中,关于全景式解析脑连接图谱和功能动态图谱的研究成为重点研究方向,而如何打破尺度壁垒,融合微观神经元和神经突触活动与大脑整体的信息处理和个体行为信息,是领域内亟待解决的一个关键挑战。2021年1月6日,由北京大学分子医学研究所牵头,联合北大信息科学技术学院电子学系、工学院以及中国人民******医学科学院等组成的跨学科团队,在NatureMethods在线发表题为“Miniaturetwo-photonmicroscopyforenlargedfield-of-view,multi-plane,andlong-termbrainimaging”的文章。文中报道了第二代微型化双光子荧光显微镜FHIRM-TPM2.0,其成像视野是该团队于2017年发布的低1代微型化显微镜的7.8倍,同时具备三维成像能力,获取了小鼠在自由运动行为中大脑三维区域内上千个神经元清晰稳定的动态功能图像,并且实现了针对同一批神经元长达一个月的追踪记录。布鲁克双光子显微镜成像原理