RIP实验将RNA反转录成cDNA的方法:
标记适当数量的0.2mLPCR管,以供分析的样本数量,并放在冰上。
将9μL(至多2μg)的RNA加入PCR管中,放在冰上。
在每个PCR反应管的在冰上加入适量的试剂。
将PCR反应管置于热循环器中。
启动以下RT反应程序:37℃,1h;95℃,5min,4℃保存。
取下PCR管。用180μL无核酸酶水(稀释10倍)稀释产物。产物可以存储在-20°C。
广州基云生物,在IP互作组检测和关键机制分子筛选验证领域,具有丰富的经验,助力您的互作机制研究。 RIP-seq和RIP-qPCR实验有哪些异同点。上海RNA蛋白互作检测RIP Sequence检测

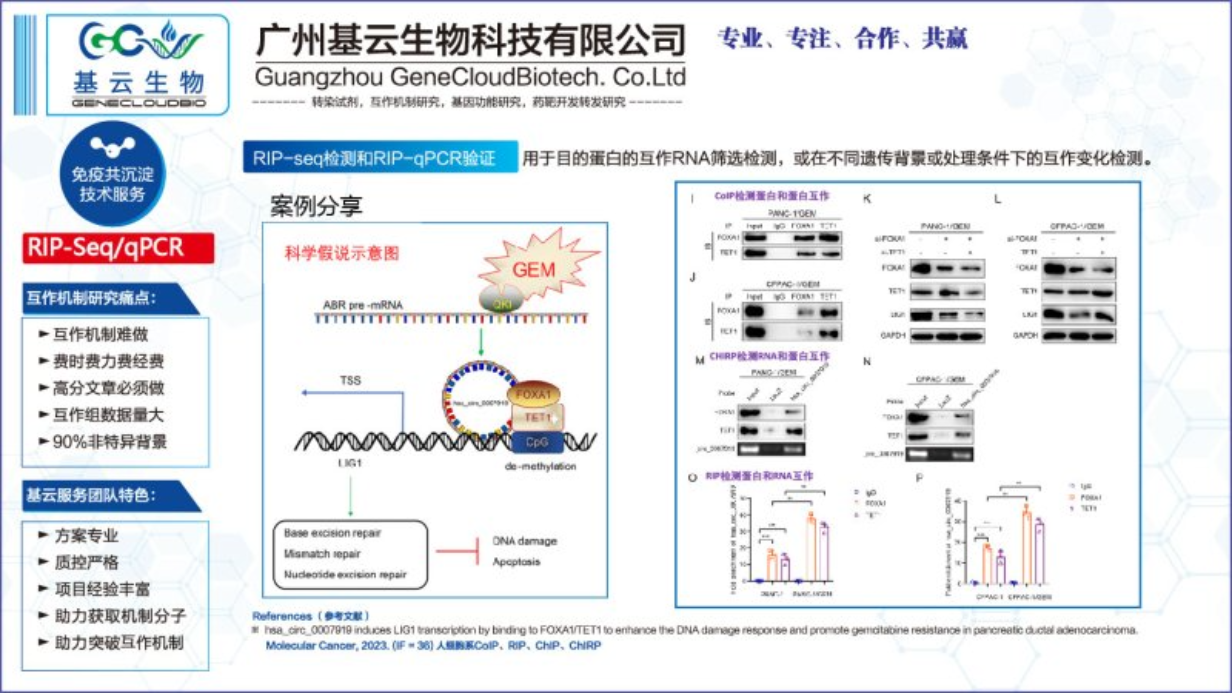
RIP-Seq检测和RIP-qPCR验证优劣势:优势:高通量获得目的蛋白的专属RNA互作库,获得目的蛋白的互作RNA机制分子。劣势:RIP-Seq的RNA库鱼龙混杂,包含目的蛋白的直接/间接的互作RNA,非特异结合,残留RNA。RIP-Seq技术和分析门槛高;RIP-qPCR验证成功率低,导致研发进展反复跌宕、时间和经费成本占用较大,严重影响士气。该项目的成功实施,比较依赖成熟和有分析经验的团队,强烈建议整包交给专业的服务商开展检测。
广州基云专注互作机制研究,致力于让实验更简单高效。 内蒙古RNA免疫共沉淀检测RIP PCR检测RIP-qPCR可以特异性地识别并结合目标RNA结合蛋白(RBP),分析与其结合的RNA分子。
RIP实验RNA纯化方法:
制备蛋白酶K缓冲液。每个免疫沉淀需要150µL蛋白酶K缓冲液,包含117µLRIP洗涤缓冲液,15µL10%SDS,18µL10mg/mL蛋白酶K。
在150µL的蛋白酶K缓冲液中悬浮每个免疫沉淀。
将第三节第4步的input样品解冻,在试管中加入107µLRIP洗涤缓冲液、15µL10%SDS和18µL蛋白酶K,使体积提高到150µL。
将所有试管在55°C下摇晃孵育30分钟以消化蛋白质。
孵育后,将管短暂离心,并将管放置在磁分离器上。将上清液转移到一个新的试管中。
在上清液的试管中加入250µLRIP洗涤缓冲液。
在每根试管中加入400µL的苯酚:氯仿:异戊醇。涡旋15秒,在室温下以14000rpm离心10分钟,以分离相位。
取出350μL水相,将其放入新管中。加入400µL的氯仿。涡旋15秒,在室温下以14000rpm离心10分钟,以分离相位。
取出300μL的水相,然后放入一个新的试管中。
在每根试管中加入50µL盐溶液I、15µL盐溶液II、5µL沉淀增强剂和850µL无水乙醇。混合并在-80°C下保持1小时至过夜,以沉淀RNA。
在4°C下以14000rpm离心30分钟,小心丢弃上清液。
用80%的乙醇清洗沉淀一次。在4°C下以14000rpm离心15分钟。小心地弃出上清液,晾干沉淀。重新悬浮在10到20µL的无RNase的水中,并将管子放在冰上。
做好RIP实验,应注意以下常见问题。1. 样本质量问题:确保使用的细胞或组织样本新鲜且未受污染,避免使用已经降解或变性的样本,这会影响RNA与蛋白质的相互作用,从而影响实验结果。2. 抗体选择:选择高特异性、高亲和力的抗体进行免疫沉淀是关键。使用非特异性抗体可能导致实验结果不准确,出现假阳性或假阴性。3. 洗涤步骤:在免疫沉淀后,充分的洗涤步骤至关重要,以去除非特异性结合的分子,减少背景噪音。4. RNase污染:由于RIP实验涉及RNA,因此必须严格避免RNase的污染。使用无RNase的试剂和耗材,并在洁净的环境中操作。5. 对照设置:设置适当的对照实验是必要的,如使用非特异性抗体作为阴性对照,或使用已知与目标蛋白结合的RNA作为阳性对照。6. 数据解读:在数据分析时,应注意识别并排除异常值,使用适当的统计方法进行分析。同时,对于不符合预期的结果,应进行重复实验以验证其真实性。综上所述,做好RIP实验需要注意样本质量、抗体选择、洗涤步骤、避免RNase污染、对照设置以及数据解读等常见问题。通过仔细考虑和遵循这些注意事项,可以提高实验的准确性和可靠性。做好RIP实验,应注意哪些常见问题。
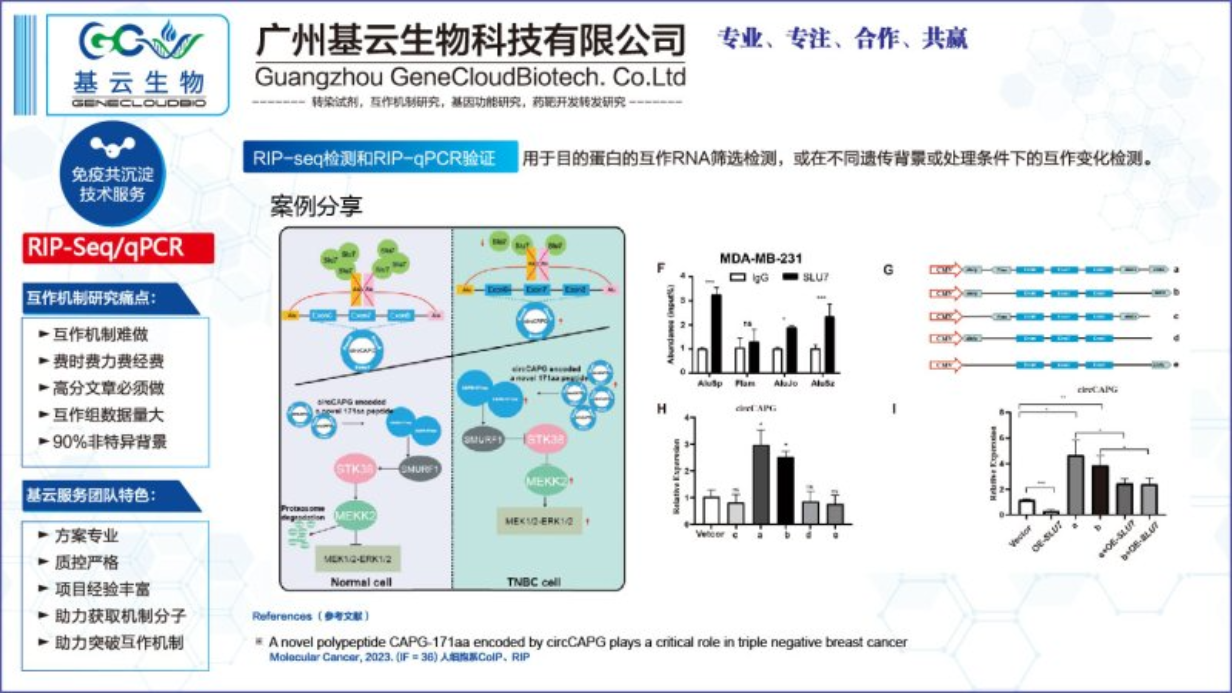
RIP-Seq检测和RIP-qPCR验证要点:
实验设计:尽量进行实验组别设计和生物学重复检测,提高后续验证的阳性率。常规过表达单组(AbIPvsIgGIP);动态互作组学(实验组vs对照组vsIgG组)。根据目的设计适当的生物学重复。如果后续以RIP-Seq数据进行互作组标准分析,则需要3-4组生物学重复;如果后续以寻找关键互作RNA,进行深入的机制研究,则建议1-2次生物学重复。经验显示单次重复假阳性率达90%。RIP-Seq强烈建议设置实验组别和生物学重复检测。
蛋白表达和细胞量:细胞用量要不少于5e7(金标准:320g离心细胞量50μl,保障项目用量)。本底低表达蛋白,建议使用过表达组进行检测。蛋白表达可根据WB结果或初步根据数据库判定。
抗体关键质控:抗体特异性与亲和效价要求高,尽量采用标签抗体或经过CoIP效果验证的抗体。抗体质量参差不齐(WB能检测到预期条带不到1/2,能检测到良好结果的不到1/4)和存在非特异性结合(几乎所有的抗体都存在非特异结合,部分非特异结合条带远大于目的条带),RIP-Seq需做WB和IP-WB质控。抗体可参考数据库。
互作蛋白筛选和验证:数据分析以信号强度作为强阳筛选,以文献查阅,功能匹配,批量RIP-qPCR验证,提高验证成功率。 在RIP-qPCR过程中,避免假阳性结果的出现是至关重要的,如何减少假阳性的风险。上海RNA蛋白互作RIP测序
进行RIP-qPCR实验,应该注意哪些关键问题,以确保实验的成功和准确性。上海RNA蛋白互作检测RIP Sequence检测
RIP(RNA结合蛋白免疫沉淀)和ChIP(染色质免疫沉淀)实验在多个方面存在明显的区别:研究对象:RIP实验主要研究细胞内RNA与蛋白质的相互作用,关注RNA结合蛋白与特定RNA分子的结合情况。ChIP实验则主要关注DNA与蛋白质的相互作用,特别是染色质上的蛋白质与DNA序列的结合。实验原理:RIP实验基于RNA分子与RNA结合蛋白在特定条件下(如紫外照射下)可以发生耦联效应。通过利用特异性抗体将RNA-蛋白质复合物沉淀下来,然后回收其中的RNA进行分析。ChIP实验则是利用特异性抗体与染色质上的蛋白质结合,然后通过洗涤和洗脱步骤将结合的DNA纯化出来,进行高通量测序或其他分析。技术应用:RIP实验是研究转录后调控网络动态过程的有力工具,可以帮助发现miRNA的调节靶点。ChIP实验则常用于研究基因表达调控、转录因子结合位点、染色质修饰等。综上所述,RIP和ChIP实验在研究对象、实验原理、实验操作、优化条件和技术应用等方面存在明显差异。上海RNA蛋白互作检测RIP Sequence检测