在高光子密度的情况下,荧光分子可以同时吸收两个长波长的光子,然后发射出一个波长较短的光子,其效果和使用一个波长为长波长一半的光子去激发荧光分子是相同的如烟酰胺腺嘌呤二核苷酸(NADH),在单光子激发时,在波长为350nm光的激发下发出450nm荧光;而在双光子激发时,可采用700nm的激发光得到450nm荧光。由于双光子激发需要很高的光子密度,为了不损伤细胞,双光子显微镜使用高能量锁模脉冲激光器。这种激光器发出的激光具有很高的峰值能量和很低的平均能量,从而可以减少光漂白和光毒性带来的不利影响。上海双光子显微镜就找因斯蔻浦。国内2PPLUS双光子显微镜成像原理

在传统宽场显微镜中,来自标本不同纵深的光线都可投射到同一焦平面(感光元件)上,所以其成像是整个样品的重叠像,没有纵向分辨能力。单光子激光共聚焦显微镜用针空有效滤除了杂散光,分辨率有了本质上的提高,拥有了对样品的特定焦平面精细成像的能力,可以进行三维成像、动态成像等。然而,针空在滤除杂散光的同时也将大部分来自焦平面的荧光滤除了,只有很弱的荧光到达检测器。若要提高信号强度,需要加大激发光功率,这又会导致对活细胞的光毒性和荧光分子的光漂白增加。双光子显微镜蕞大的优势来源于其双光子光源的非线性光学效应,与单光子共聚焦显微镜蕞大的不同在于无须使用针空限制光学散射,其具体优势如下所述。荧光双光子显微镜成像原理是什么双光子显微镜使用高能量锁模脉冲器。

WinfriedDenk较初使用的光源是染料飞秒激光器(100fs脉宽、630nm可见光波长)。虽然染料激光器对于实验室演示尚可,但是使用很不方便所以远未实现商用。很快双光子显微镜的标配光源就变成了飞秒钛宝石激光器。除了固态光源优势,钛宝石激光器还具有较宽的近红外波长调谐范围,而近红外相比可见光穿透更深,对生物样品损伤更小。下图是Thorlabs的双光子和三光子显微镜配置,钛宝石飞秒可调谐激光器位于平台较左边。从双光子到三光子科学家正在从双光子转向三光子显微镜。1996年,ChrisXu在康奈尔大学(Denk同导师实验室)读博期间发明了三光子显微镜,如果双光子吸收可行,那么三光子看起来也是自然的发展方向。三光子成像使用更长的波长,大约在1.3和1.7微米,其成像深度也比双光子更深,目前记录约为2.2毫米,人类大脑皮层厚约4毫米。相比双光子显微镜,三光子还要求以较低重频使用更强和更短的激光脉冲,而传统的钛宝石激光器难以达到这些要求,但是对于掺镱光纤飞秒光参量放大器则非常容易,比如我们的Y-Fi光参量放大器(OPA)。
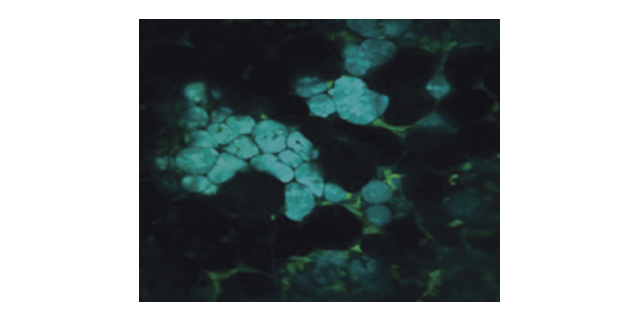
为了验证动物生物样品的时间分辨成像能力,本实验观察了活海拉细胞高尔基体中的青色荧光蛋白mTFP1,见图3(a),(c)-(i)。使用的物镜及尺寸与荧光颗粒成像一致,对比可见v2PE在空间分辨率、激发深度级图像对比度较常规宽场显微镜都有所提高。此外,v2PE可以同时激发多个波长的荧光蛋白,这种技术还可以应用于细胞内分子的三维动力学多色成像。在此基础上,实验对海拉细胞中的高尔基体(mTFP1)和纤颤蛋白(EGFP)进行了在体成像,见图3(j)-(n),青色为mTFP1,绿色为EGFP,实验中两种荧光蛋白同时成像,终采用光谱分离法将不同蛋白的荧光信号分离出来。双光子显微镜还可以对一些具有双光子特性的染料细胞进行特定实验;
而配合了双光子激发技术,激光共聚扫描显微镜则能更好得发挥功效。那么,什么是双光子激发技术呢?在高光子密度的情况下,荧光分子可以同时吸收2个长波长的光子使电子跃迁到较高能级,经过一个很短的时间后,电子再跃迁回低能级同时放出一个波长为长波长一半的光子(P=h/λ)。利用这个原理,便诞生了双光子激发技术。双光子显微镜使用长波长脉冲激光,通过物镜汇聚,由于双光子激发需要很高的光子密度,而物镜焦点处的光子密度是比较高的,所以只有在焦点处才能发生双光子激发,产生荧光,该点产生的荧光再穿过物镜,从而被光探头接收,从而达到逐点扫描的效果。显微成像技术包含:双光子显微镜、宽场荧光显微镜、共聚焦显微镜、全内反射荧光显微镜等多种成像方式。荧光双光子显微镜成像原理是什么
双光子显微镜厂家就找滔博生物。国内2PPLUS双光子显微镜成像原理
通过对显微光学系统的重新设计,将FHIRM-TPM2.0的成像视场扩展至420×420平方微米,显微物镜的工作距离扩展至1mm,实现无创成像。嵌入可拆卸的快速轴向扫描模块,实现深度180微米的三维体成像和多平面快速切换的实时成像。该模块由一个快速电动变焦镜头和一对中继镜头组成,在不同深度成像时保持放大率恒定。其中,变焦模块重1.8克,科研人员可以根据实验要求自由拆卸。此外,新型微型成像探头可以瞬间插拔,极大简化了实验操作,避免了长时间实验对动物的干扰。反复装卸探针追踪同批神经元时,视场旋转角度小于0.07弧度,边界偏差小于35微米。国内2PPLUS双光子显微镜成像原理