企业商机
支原体基本参数
- 品牌
- 世途科生物
- 型号
- CM0001
支原体企业商机
一步法快速支原体检测的原理主要基于等温扩增技术,这是一种在恒定温度下进行的核酸扩增方法。以下是具体的步骤和原理:
1. 等温扩增技术:一步法快速支原体检测试剂盒利用LAMP(Loop-Mediated Isothermal Amplification,环介导等温扩增)技术或类似的等温扩增技术。这些技术允许在恒定温度下进行DNA的快速扩增,通常在60-65°C之间。
2. 特异性引物:该方法使用设计好的特异性引物,这些引物靶向支原体DNA的保守区域。引物的设计确保了扩增过程的特异性,从而减少非目标序列的扩增。
3. 快速扩增:在适宜的条件下,等温扩增技术可以在15至60分钟内实现高达10^9至10^10倍的核酸扩增,从而快速检测出支原体的存在。
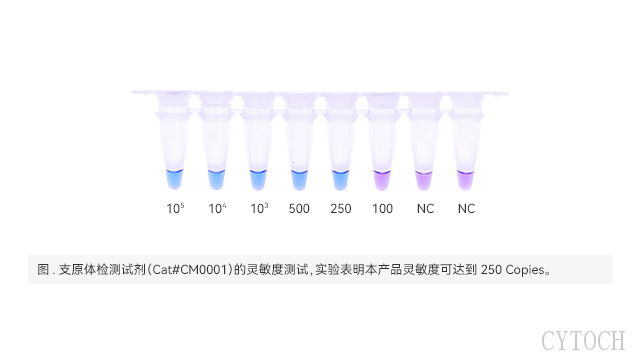
4. 颜色变化指示:一步法试剂盒中通常包含有颜色指示剂,当支原体DNA被扩增时,反应液的颜色会发生变化,从而可以通过肉眼直接观察到检测结果。例如,从蓝紫色变为天蓝色,表示样本中存在支原体。
5. 操作简便:一步法支原体检测不需要复杂的设备,通常只需要水浴锅或PCR仪即可完成操作,使得检测过程更加简便快捷。
支原体去除之后对细胞转染有无影响?深圳细胞支原体检测时间
细胞培养中支原体检测出现假阳性结果可能由以下原因引起:
1. 扩增产物污染:PCR扩增产生的大量DNA拷贝若未妥善处理,极微量的污染就可能导致假阳性结果。
2. 引物设计不当:引物设计不够特异性,可能会与非目标序列发生反应,导致非特异性扩增。
3. 试剂质量问题:使用的dNTPs、引物、DNA聚合酶等试剂质量不佳,可能引起非特异性扩增或假阳性结果。
4. 操作技术问题:实验操作不规范,如混合样本、标签错误或样本标识不清等,可能导致假阳性结果。
5. PCR反应条件设置不当:不恰当的PCR反应条件,如温度和时间选择不当,可能导致非特异性扩增。
6. DNA污染:PCR环境中的DNA污染会干扰结果,导致假阳性
细胞培养支原体检测说明书细胞培养过程中支原体污染怎么预防?
支原体预防的实验步骤主要包括以下几个方面:
1. 无菌操作技术:在细胞培养过程中,严格遵守无菌操作规程,包括穿戴适当的实验服、手套,使用无菌工具和耗材。
2. 环境控制:保持实验室环境清洁,定期消毒工作台和实验室表面,使用层流罩或生物安全柜进行细胞操作。
3. 细胞培养基和试剂的无菌过滤:所有加入到细胞培养基中的试剂和补充物,如血清、抗*素等,都应通过无菌过滤以去除支原体。
4. 细胞培养基和试剂的检测:在添加到细胞培养物之前,对新的细胞培养基和试剂进行支原体检测,以确保它们没有被污染。
5. 定期检测:即使采取了预防措施,也应定期对细胞培养物进行支原体检测,以确保及时发现并处理潜在的污染。
6. 避免交叉污染:避免从一个细胞培养物到另一个的交叉污染,使用的移液器和工具,避免在不同细胞培养物之间重复使用。
7. 细胞培养物的筛选:使用已知无支原体污染的细胞株进行实验,或者在开始实验前对细胞株进行筛选。
8. 使用预防性试剂:在某些情况下,可以在细胞培养过程中添加特定的预防性试剂,如支原体预防剂,以降低污染风险。
支原体去除的实验步骤通常包括以下几个阶段:
1. 支原体检测:在进行去除之前,首先要确认细胞培养物是否受到支原体污染。这可以通过多种方法实现,如PCR法、LAMP法或支原体培养法。
2. 选择合适的去除试剂:一旦确认存在支原体污染,需要选择一种有效的去除试剂。
3. 去除试剂的添加:根据去除试剂的说明书,将试剂添加到受污染的细胞培养基中。通常,这涉及到将一定比例的去除试剂加入到细胞培养液中。
4. 孵育:添加去除试剂后,将细胞培养物放回培养箱中孵育。孵育时间和条件(如温度、CO2浓度)应根据试剂的推荐进行调整。
5. 监测去除效果:在孵育过程中,定期监测细胞的状态和去除效果。这可能包括观察细胞形态、生长速率的变化,以及通过显微镜检查是否有支原体存在的迹象。
6. 后续检测:去除过程完成后,再次使用支原体检测方法确认污染是否已被成功。
支原体去除的实验步骤?
细胞培养中支原体难以彻底消灭的原因主要包括以下几点:
1. 无细胞壁结构:支原体是没有细胞壁的微生物,这使得许多作用于细胞壁的抗*素对支原体无效。
2. 微小体积:支原体体积小,能够穿过常规的除菌滤膜,例如0.20微米甚至0.10微米的滤膜。
3. 隐匿性:支原体污染初期很难被察觉,它们在普通光学显微镜下几乎不可见,因此细胞被支原体污染后,前期很难被发现。
4. 传播途径多样:支原体可以通过细胞培养物、细胞悬液、细胞培养用具等途径迅速传播。
5. 污染源 :支原体污染源包括细胞间的交叉污染、操作人员的口腔、皮肤,以及细胞培养用的组分如血清、培养液等。
6. 环境因素:实验室环境、试验台、超净台、培养箱等可能被支原体污染,引起细胞的污染。
7. 抗*素耐药性:支原体可能对某些抗*素产生耐药性,使得治*效果变差。
8. 检测和清理方法的局限性:一些传统的支原体检测和清理方法可能不够灵敏或有效,导致难以彻底清理支原体
如何检测新鲜的培养基是否有支原体污染?杭州支原体预防多少钱对于同一个样品,为什么一步法恒温试剂盒检测结果为阳性,而PCR检测为阴性呢?深圳细胞支原体检测时间
qPCR法,即定量聚合酶链式反应(Quantitative Polymerase Chain Reaction)法,是一种高度灵敏和特异的分子生物学技术,用于检测和定量DNA序列。在支原体检测中,qPCR法的原理主要包括以下几个步骤:
1. DNA提取:首先从待测样本中提取DNA,这可能包括细胞培养上清液或组织样本中的支原体DNA。
2. 设计特异性引物:针对支原体的保守DNA序列,如16S rRNA基因,设计特异性的DNA引物。
3. 荧光标记探针:使用荧光标记的探针,该探针与目标DNA序列互补,能够在PCR扩增过程中与扩增的DNA结合。
4. Ct值确定:Ct值(阈值循环数)是指在PCR反应中,荧光信号强度超过预定阈值的循环次数。Ct值越低,表示样本中支原体DNA的量越多。
5. 定量分析:通过标准曲线法或相对定量法,将Ct值转换为支原体DNA的定量结果。
qPCR法的优势在于其高灵敏度和特异性,能够检测到非常低水平的支原体污染,并且可以在短时间内提供结果,这对于需要快速检测的生物制品生产和细胞培养质量控制非常重要
深圳细胞支原体检测时间
与支原体相关的文章
温州支原体检测方法bst
2024-11-27
随着科技的不断进步,支原体检测技术也在持续创新和发展。新的检测技术和方法不断涌现,为我们提供了更加便捷、高效和准确的检测手段。同时,检测设备的不断升级和优化,也使得支原体检测能够更加地应用于临床诊断和科研实践中。总之,支原体检测作为洞察微观世界的健康卫士,在医学和科研领域都发挥着不可或缺的重要作用。我们应当重视支原体检测技术的发展和应用,不断提高检测水平,让这一微观世界的“侦察兵”为我们的健康和科学研究事业提供更加坚实的保障。细胞培养中,支原体检测必不可少,能防止支原体污染,保障细胞培养质量。温州支原体检测方法bst在微生物的世界里,支原体是一种独特而神秘的存在。支原体极其微小,小到常常让人忽...
- 温州支原体去除多少钱 2024-11-27
- 温州支原体检测方法恒温扩增 2024-11-27
- 广州支原体去除试剂多少钱 2024-11-26
- 上海细胞支原体检测要多久 2024-11-26
- 杭州细胞培养支原体检测时间 2024-11-26
- 温州细胞培养支原体预防试剂货期 2024-11-26
- 上海细胞支原体检测如何取样 2024-11-26
- 南京细胞支原体污染 2024-11-26
- 杭州细胞支原体去除试剂现货 2024-11-26
- 杭州支原体检测如何取样 2024-11-26
与支原体相关的产品
与支原体相关的问题
与支原体相关的热门
- 苏州细胞培养支原体检测方法PCR法 2024-11-26
- 南京细胞支原体检测试剂货期 2024-11-25
- 广州细胞支原体预防货期 2024-11-25
- 深圳支原体检测试剂货期 2024-11-25
- 细胞培养支原体检测说明书 2024-11-25
- 杭州细胞培养支原体检测试剂现货 2024-11-25
产品推荐

温州支原体检测方法bst
2024-11-27
南京anti DYKDDDDK免疫沉淀磁珠的选择
2024-11-27
温州支原体去除多少钱
2024-11-27
上海RIP免疫沉淀磁珠原理
2024-11-27
温州支原体检测方法恒温扩增
2024-11-27
相关资讯

- RIP免疫沉淀磁珠原理 11-27
- 广州anti DYKDDDDK免疫沉淀实验原理 11-27
- 北京Co IP免疫沉淀磁珠原理 11-27
- 北京Protein AG免疫沉淀外包公司 11-27
- 南京蛋白免疫沉淀磁珠原理 11-27
- 广州支原体去除试剂多少钱 11-26
- 上海细胞支原体检测要多久 11-26
- 杭州细胞培养支原体检测时间 11-26
- 苏州Co IP免疫沉淀磁珠应用 11-26
- 温州细胞培养支原体预防试剂货期 11-26