子宫内膜异位症模型异位灶的形成需要有血管的建立来提供能量。血管内皮细胞因子(VEGF)是一种多功能的细胞因子,它可促进血管内皮细胞增殖。黄荷凤[口]将EM患者的子宫内膜种植到ICR小鼠腹腔内,移植后3d内,移植的内膜细胞只能够通过腹腔液或者临近组织得到部分的氧和营养物质,所以受到了缺血缺氧等的剌激,从而诱导了VEGF的强表达,使它明显高于手术前,通过诱导血管形成及组织重构来满足继续生长。VanLangendonckt[四]等将月经期内膜加入血清或红细胞接种于裸鼠腹腔,观察到间质中含铁血黄素沉积。认为经血中红细胞是形成含铁血黄素的原因,也是引起慢性炎症和氧化损伤的因素之一,从而诱导VEGF等的表达,通过促使新生血管的形成参与了EM的病理研究人员正在利用子宫内膜异位症模型寻找新的改善靶点。河北小鼠子宫内膜异位症模型如何构建
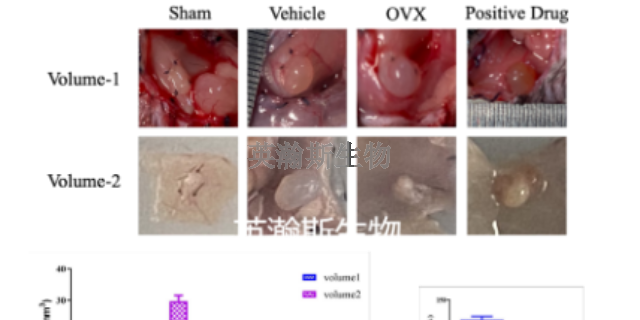
子宫内膜异位症模型的观察指标验证模型是否成功:大鼠建模28d后再次手术,腹腔麻醉后固定,腹部备皮,消毒铺巾,取原切口旁开腹,取出3个不同部位的移植物。记录移植物大体特点。用游标卡尺测量移植物的长度、高度与宽度,按公式计算体积:体积=0.52×长×宽×高[4]。用电子天平称取移植物质量。将取出的移植物和左侧子宫的在位内膜标本用10%多聚甲醛固定,常规石蜡包埋,H-E染色,显微镜下观察组织病理学变化来验证模型的成功率。辽宁哪里有子宫内膜异位症模型动物实验外包子宫内膜异位症模型是研究该疾病发病机理的重要工具。
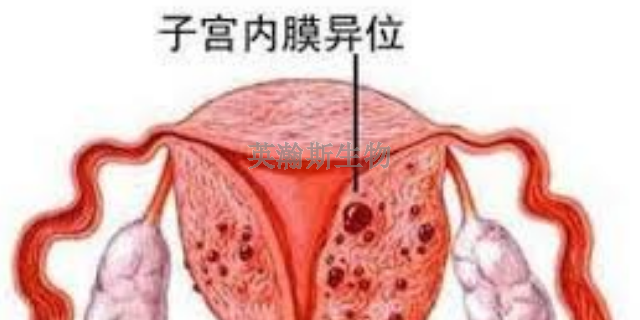
采用自体移植方法建立子宫内膜异位症大鼠模型,比较不同移植部位的建模效果。方法 取40只雌性、成熟未交配SD大鼠,将自体子宫内膜组织分别移植于卵巢、宫骶韧带及腹壁上,术后28 d手术取出移植物,测量移植物的体积和质量,对移植物进行组织形态学观察并比较不同部位的成模率。结果 卵巢部位移植物体积和质量大于其他两个部位(P<0.05),而宫骶韧带及腹壁部位的移植物体积及质量差异无统计学意义。3个不同部位的成模率差异无统计学意义,且移植物组织病理学相似。结论 卵巢、宫骶韧带及腹壁3个部位的自体子宫移植均可建立子宫内膜异位症模型,病理改变与子宫内膜异位症患者相似,但卵巢部位建模效果比较好,更有利于子宫内膜异位症新的治疗方法的开发及研究。
研究人员正在不断优化子宫内膜异位症模型,以提高其实验准确性,这是一项至关重要的工作。他们深知,一个精确的模型能够更真实地反映疾病的发病机制和病理变化,从而为后续的实验研究和临床改善提供更为可靠的依据。为了实现这一目标,研究人员不断尝试新的实验方法和技术,对模型的构建过程进行精细化调整,以确保每一个细节都能得到精细控制。同时,他们还积极与同行进行交流和合作,共同推动子宫内膜异位症模型的研究进展。这些努力不仅有助于提升实验结果的准确性,也为推动妇科医学的发展提供了有力的支持。相信在不久的将来,通过不断优化子宫内膜异位症模型,我们将能够更深入地了解这一疾病,为更多患者带来福音。该模型可以帮助我们理解子宫内膜异位症在不同人群中的差异表现。
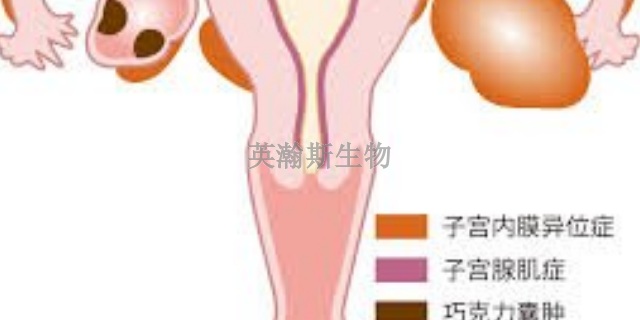
子宫内膜异位症模型作为研究疾病进展和预后的有效工具,其在妇科医学领域的应用价值不容忽视。通过构建高度仿真的子宫内膜异位症模型,我们能够在实验室环境下模拟疾病的发展过程,从而深入观察并了解疾病的进展机制和预后情况。这一模型不仅能够为我们提供关于疾病发生、发展和转归的直观证据,还能帮助我们评估不同治疗方案对疾病进展和预后的影响,为制定个性化的治疗方案提供科学依据。因此,子宫内膜异位症模型的研究不仅有助于我们更深入地了解疾病的本质,还能为改善患者的预后和生活质量提供有力支持。子宫内膜异位症模型的优化有助于我们更好地模拟疾病的自然发展过程。推荐的子宫内膜异位症模型造模方法
大鼠子宫内膜异位症模型怎么做?河北小鼠子宫内膜异位症模型如何构建
子宫内膜异位症模型的建立无疑为生殖健康领域的进步注入了新的动力。这一模型的精细模拟与高度仿真,使得研究人员能够更深入地了解子宫内膜异位症的发病机理、病理过程及其对生殖系统的影响,从而为疾病的预防、诊断和改善提供了更为科学的依据。同时,该模型也为生殖健康领域的研究人员提供了一个全新的实验平台,有助于加速相关研究成果的转化与应用。因此,可以说子宫内膜异位症模型的建立,不仅为疾病研究提供了重要的工具,更推动了生殖健康领域的快速发展,为广大女性的健康福祉贡献了力量。河北小鼠子宫内膜异位症模型如何构建