- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
作为一种分子通断开关的KRAS发生突变时会处于“开启”状态。在80%~95%的胰腺导管腺病(PDAC)当中,这个基因发生突变,这也是这种一些疾病中较为常见的突变。这些研究人员证实iExosome能够运送特异性地靶向KRAS的siRNA和shRNA分子,并且比他们的合成对应物脂质体(liposome)更加高效。脂质体不具有外泌体表现出的天然复杂性和优势。德州大学MD安德森一些疾病中心一些疾病生物学助理教授ValerieLeBleu博士说,“我们的研究提示着与脂质体相比,外泌体表现出运送siRNA分子和压制侵袭性胰腺瘤生长的优异能力。我们也证实外泌体表面上的CD47存在允许它们躲避来自循环单核细胞的吞噬作用。外泌体提取:根据外泌体的大小,从蛋白质和其他大分子中分离外泌体。太原外泌体提取试剂直销价
外泌体在肺病进程中的作用:在一些病症微环境中,一些病症细胞来源的外泌体能够诱导CD4+T分化为调节性T细胞,压制机体的抗一些病症免疫反应;肺病细胞分泌的外泌体含有miR-21和miR-29a,可在免疫细胞中结合并启动TLR8,使TLR介导的NF-κB信号通路活化,从而导致一些病症的生长和转移。在肺病的侵袭和转移过程中,细胞间通讯扮演着重要的角色。据有关报道称,NSCLC分泌的外泌体内TGFβ和IL10的高表达与肺病的转移密切相关。此外,启动的T细胞可以通过调控Fas信号通路增加基质金属蛋白酶9(MMP9)的表达,进而促进肺病的转移。这些机制有望成为肺病治病的潜在靶点。虽然大多数外泌体都是促进一些病症的侵袭与转移,但也有报道称,外泌体miR-302b可以通过压制TGFβRⅡ来压制肺病细胞的转移与增殖。如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物。上海外泌体提取试剂厂家外泌体提取:可用于收集大于800nm、400nm或200nm的外泌体。

外泌体相关技术在过去几年一直在快速发展,预计市场将大幅增长,因为它们可被应用到液体活检、精细医学和再生医学领域。特别是,一些疾病衍生的外泌体通过调节血管生成、转移和免疫来影响细胞的侵袭性,使其成为用于一些疾病检测、诊断和治病选择的极其有用的生物标志物来源。在风险投资方面,有很多市场活动。2016年1月,ExosomeDiagnostics公司在B轮融资中获得6000万美元资金,并于2017年7月获得3000万美元的C轮融资。同样,CodiakBiosciences公司于2016年由MDAnderson一些疾病中心与两家风险投资公司共同成立,以8000多万美元的A和B轮融资成立该公司。2017年11月29日,CodiakBioSciences公司又增加了7650万美元的C轮融资。在整个A、B和C轮融资中,CodiakBioSciences公司募集了惊人的1.685亿美元。
外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集菌类,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等,因此发表文章时易受质疑。如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物。外泌体提取:小分子可进入凝胶中绝大部分孔洞,在柱中受到更强地滞留,更慢地被洗脱出。

外泌体的提取方法学规范、统一定量及鉴定等。关于外泌体的提取有超速离心、试剂盒、超滤法、蔗糖密度梯度离心等,然而各种方法均有其利弊。超速离心法是目前外泌体相关文章中的主流方法,由于离心步骤繁琐,费事费力,而且步骤多导致实验中容易污染,且损耗量大,使得较终回收的外泌体不稳定。而且对于抽提细胞上清来说,更是极为不请便,试想用提取300ml的上清需要6个50ml离心管,无论是过滤还是后续的每一步的离心去沉淀,都具有操作极其不便的缺点,总之非常麻烦。而超滤法存在外泌体会堵塞膜孔,造成浓缩效率低,浓缩管重复利用差,甚至堵塞在膜孔的外泌体还可能会粘连成团,造成损失及较后的数据有误差,对于后续实验也有影响外泌体提纯试剂盒的特色与优势:无需耗时的超速离心,过滤或特殊注射器。温州外泌体提取试剂推荐厂家
外泌体提取:回收率不稳定(可能与转子类型有关),纯度也受到质疑。太原外泌体提取试剂直销价
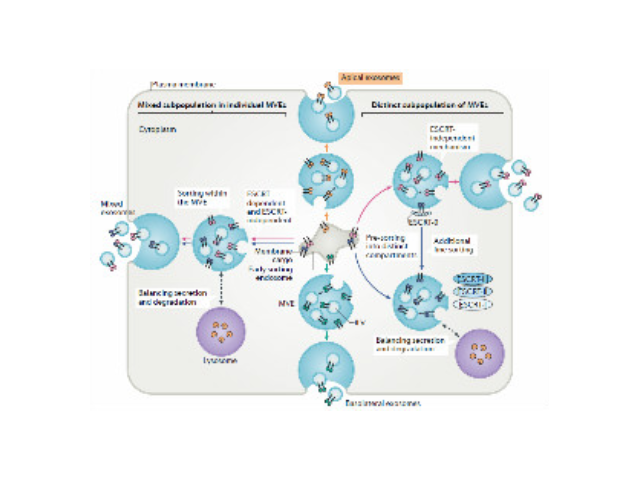
外泌体的形成与鉴定:首先,细胞膜内陷形成一个杯状结构,包括细胞表面蛋白和与细胞外环境相关的可溶性蛋白,导致早期胞内体(early-sortingendosome,ESE)的从头形成,或者是杯状结构直接和已经存在的ESEs融合;trans-高尔基体和内质网也能协助形成ESEs。ESE成熟后形成晚期胞内体(late-sortingendosomes,LSEs),较终形成MVBs(也称为多囊内小体)。MVBs是通过endosome限制膜向内凹(即质膜双凹)形成的,这一过程导致MVBs含有多个ILVs。MVB可以与溶酶体或自噬体融合,较终降解或与质膜融合释放作为外泌体的ILVs。外泌体表面蛋白包括四聚体蛋白、整合蛋白、免疫调节蛋白等。外泌体可以包含不同类型的细胞表面蛋白、细胞内蛋白、RNA、DNA、氨基酸和代谢物。使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后太原外泌体提取试剂直销价
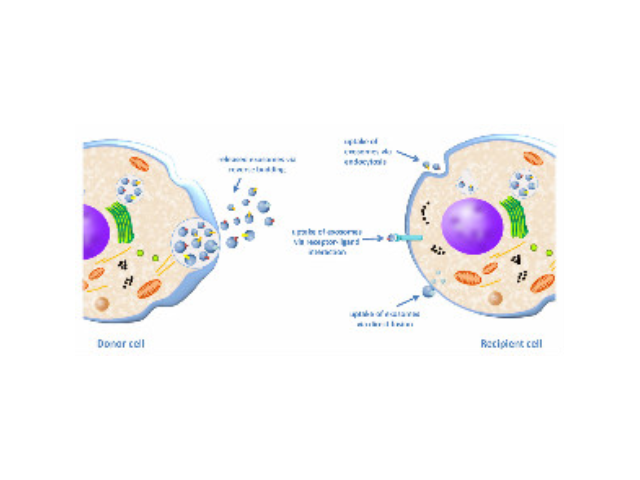
当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而启动靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而启动细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA。人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。外泌体(Exosome)发现...
- 昆明正规外泌体提取试剂报价 2024-11-14
- 长沙正规外泌体提取试剂进货价 2024-11-14
- 上海正规外泌体提取试剂哪里买 2024-11-13
- 郑州正规外泌体提取试剂厂家现货 2024-11-13
- 徐州正规外泌体提取试剂直销价 2024-11-13
- 长沙外泌体提取试剂厂家直销 2024-11-13
- 珠海外泌体提取试剂厂家直销 2024-11-13
- 南昌正规外泌体提取试剂哪家好 2024-11-13
- 太原正规外泌体提取试剂报价 2024-11-12
- 太原正规外泌体提取试剂厂家供应 2024-11-11
- 正规外泌体提取试剂销售厂家 2024-11-10
- 合肥外泌体提取试剂报价 2024-11-10
- 温州外泌体提取试剂进货价 2024-11-10
- 杭州正规外泌体提取试剂报价 2024-11-10
- 长沙外泌体提取试剂厂家批发价 2024-11-10
- 金华正规外泌体提取试剂直销厂家 2024-11-10


- 杭州正规RNA提取试剂销售厂家 11-23
- 唐山RNA提取试剂 11-23
- 青岛正规RNA提取试剂厂家批发价 11-23
- 合肥天津RNA提取试剂 11-22
- 温州RNA提取试剂厂家 11-22
- 金华RNA提取试剂直销价 11-22
- 珠海正规RNA提取试剂销售厂家 11-22
- 北京RNA提取试剂 11-22
- 昆明正规RNA提取试剂厂家推荐 11-22
- 上海正规RNA提取试剂厂家 11-22