- 品牌
- 司鼎;OriCell
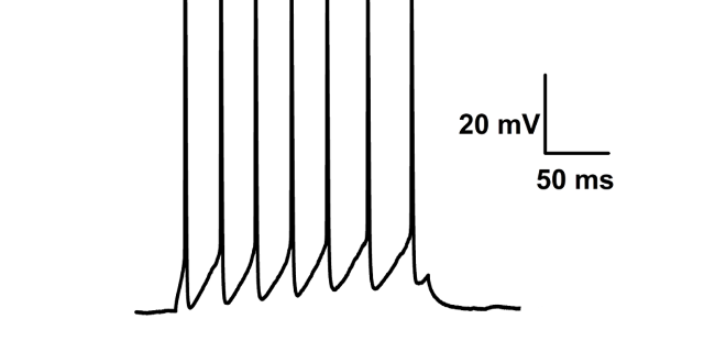
膜片钳技术是用于纪录全细胞或个别细胞膜上离子信道电生理特性的研究方法,目的在于提供基础研究知识与新药开发时研究细胞电特性或小分子药物对细胞膜上离子信道特性的影响,替开发标靶药物提供一个测试平台。传统的细胞培养膜片钳系统由人工操作,实验人员在取得元代细胞(例如心肌细胞与神经元)后,将研究对象细胞养在玻片上,以手动方式将纪录电极移动放置在胞体上方并压到细胞膜上,此时纪录电极在膜外溶液里的电阻大约为3-9 ΜΩ。膜片钳放大器是整个实验系统中的中心,它可用来作单通道或全细胞记录。东莞神经生物学膜片钳实验
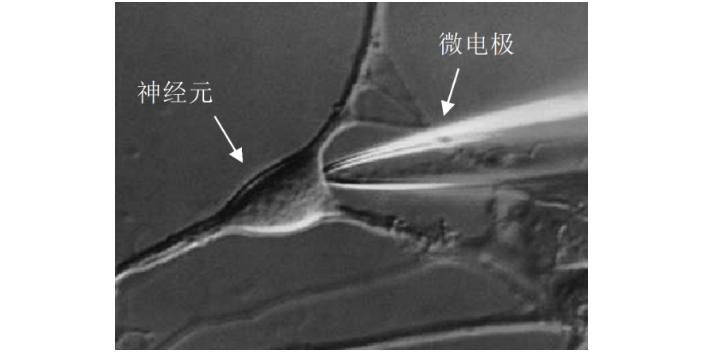
膜片钳使用操作流程及注意事项:1.实验结束后必须关闭实验室的水电,检查实验室门窗。2.凡是在本平台使用仪器的同学必须履行实验室相关要求,完成值日等相关工作(值日生按照实验室统一所发值日生要求履职)。3.在仪器使用以前及使用之后按按照使用时长做好登记工作。4.拉制仪提前预热(至少30min)。且用完及时关闭。电热加热线温度很高,在使用时注意避免烫伤。4.电脑里面的软件不得随意删改,不得在本机电脑下载别的软件,拷数据时需用实验室配置的U盘。5.禁止私拉电线,如有实验要求可与老师及时沟通。东莞神经生物学膜片钳实验膜片钳技术是电生理记录的常用手段,目前在科学研究中使用普遍。

膜片钳操作实验:标本制备根据研究目的的不同,可采用不同的细胞组织,如心肌细胞、平滑肌细胞、细胞等,现在几乎可对各种细胞进行膜片钳的研究。对所采用的细胞,必须满足实验要求,一般多采用酶解分离法,也可采用细胞培养法;另外,由于与分子生物学技术的结合,现在也运用分子克隆技术表达不同的离子通道,如利用非洲爪蟾卵母细胞表达外源性基因等。电极在实验前要灌注电极液,由于电极较细,因此在充灌前,电极内液要用0.2 μm的滤膜进行过滤。一般电极充灌可分灌尖(tipfilling)和后充两步灌尖时将电极浸入内液中5s即可。
膜片钳实验系统:根据不同的电生理实验要求,可以组建不同的实验系统,但有若干共同的基本部件,包括机械部分(防震工作台、屏蔽罩、仪器设备架)、光学部分(显微镜、视频监视器、单色光系统)、电子部件(膜片钳放大器、刺激器、数据采集的设备、计算机系统)和微操纵器在大多数膜片钳实验,要求所有实验仪器及设备均具有良好的机械稳定性,以使微电极与细胞膜之间的相对运动尽可能小。防震工作台放置倒置显微镜和与之固定连接的微操纵器,其他设备置于台外。屏蔽罩由铜丝网制成,接地以防止周围环境的杂散电场对膜片钳放大器的探头电路的干扰。仪器设备架要靠近工作台,便于测量仪器与光学仪器配接。全细胞式膜片方式使细胞内与浴槽之间的漏流极少。
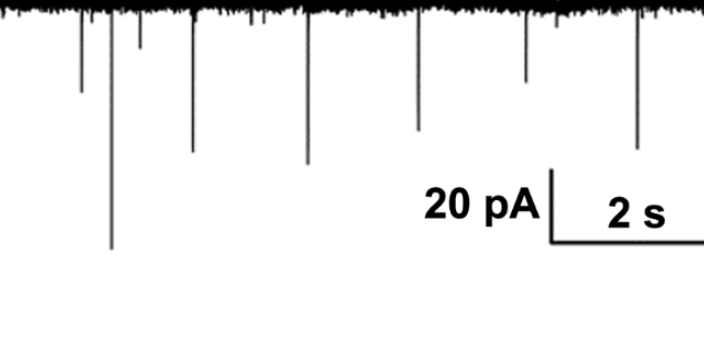
膜片钳的数据如何处理:穿孔膜片(perforated patch)是为克服常规全细胞模式的胞质渗漏问题,有学者将与离子亲和的制霉菌素或二性霉素b经微电极灌流到含有类甾醇的细胞膜上,形成只允许一价离子通过的孔,用此法在膜片上做很多导电性孔道,借此对全细胞膜电流进行记录。由于此模式的胞质渗漏极为缓慢,局部串联阻抗较常规全细胞模式高,所以钳制速度很慢,也称为缓慢全细胞模式。它适合于小细胞的电压钳位,对于直径大于30μm的细胞很难实现钳位。不足之处是由于电极与细胞间交换快,细胞内环境很容易破坏,因此记录所用的电极液应与胞浆主要成分相同,如高k+,低na+和ca2+及一定的缓冲成分和能量代谢所需的物质。膜片钳技术是一种记录通过离子通道的离子电流来反映细胞膜上离子通道分子活动的技术。东莞神经生物学膜片钳实验
膜片钳技术本质上也属于电压钳范畴。东莞神经生物学膜片钳实验
膜片钳电生理纪录系统及记录方法:细胞膜由双层脂膜组成,具有密封绝缘的特性,因此当纪录 电极接触到细胞膜时电阻会开始上升,然后以人工方式对纪录电极内施加一个负压,可以让电极与胞膜之间吸附得更为紧密而电阻也会加速上升,当纪录电极的电阻达到千兆欧姆(Giga Ω)时,意味着细胞膜与电极之间几乎没有电流漏出,之后对电极内压力施以一个快速的负压将细胞膜吸破,这样纪录电极与细胞胞体之间会形成一个封闭的电容,此时就可以开始对细胞进行实验。东莞神经生物学膜片钳实验
膜片钳技术基本原理与特点:膜片钳技术本质上也属于电压钳范畴,两者的区别关键在于:①膜电位固定的方法不同;②电位固定的细胞膜面积不同,进而所研究的离子通道数目不同。电压钳技术主要是通过保持细胞跨膜电位不变,并迅速控制其数值,以观察在不同膜电位条件下膜电流情况。因此只能用来研究整个细胞膜或一大块细胞膜上所有离子通道活动。目前电压钳主要用于巨大细胞的全性能电流的研究,特别在分子克隆的卵母细胞表达电流的鉴定中发挥着其他技术不能替代的作用。该技术的主要缺陷是必须在细胞内插入两个电极,对细胞损伤很大,在小细胞如神经元,就难以实现,又因细胞形态复杂,很难保持细胞膜各处生物特性的一致。神经元研究合作,膜片钳技...
- 广州医学膜片钳成像应用 2026-05-24
- 无锡神经生物学离子通道原理 2026-05-24
- 金华细胞生物学脑片膜片钳研究方案 2026-05-24
- 徐州医学脑片膜片钳应用 2026-05-24
- 杭州全自动电生理膜片钳服务 2026-05-24
- 芜湖医学膜片钳全细胞记录 2026-05-24
- 温州全自动脑定位膜片钳网站 2026-05-24
- 金华神经生物学离子通道原理 2026-05-24
- 东莞细胞生物学膜片钳技术研究方案 2026-05-23
- 苏州神经生物学膜片钳全细胞记录技术 2026-05-23
- 苏州全自动离子通道原理及步骤 2026-05-23
- 莆田药理学膜片钳电生理技术 2026-05-23
- 湖州细胞生物学膜片钳成像原理及步骤 2026-05-23
- 上海神经生物学膜片钳技术技术 2026-05-23
- 徐州全自动膜片钳电生理技术网站 2026-05-23
- 莆田全自动脑片膜片钳服务 2026-05-23


- 芜湖医学膜片钳全细胞记录 05-24
- 温州全自动脑定位膜片钳网站 05-24
- 金华神经生物学离子通道原理 05-24
- 东莞细胞生物学膜片钳技术研究方案 05-23
- 苏州神经生物学膜片钳全细胞记录技术 05-23
- 杭州神经生物学离子通道研究方案 05-23
- 常州全自动脑定位膜片钳技术 05-23
- 嘉兴全自动脑定位膜片钳哪家好 05-23
- 金华细胞生物学脑片膜片钳原理 05-23
- 苏州全自动离子通道原理及步骤 05-23